
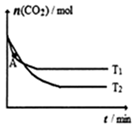
 容积固定的密闭容器中,充入一定体积的CO2和H2,发生反应:CO2(g)+3H2(g)?CH3OH (g)+H2O(g).测得不同温度下CO2的物质的量随时间变化如图.下列说法正确的是( )
容积固定的密闭容器中,充入一定体积的CO2和H2,发生反应:CO2(g)+3H2(g)?CH3OH (g)+H2O(g).测得不同温度下CO2的物质的量随时间变化如图.下列说法正确的是( )| A. | 该反应为吸热反应 | |
| B. | T1、T2对应的平衡常数K1>K2 | |
| C. | T1时,图中A点的正反应速率小于逆反应速率 | |
| D. | T2时,若上述反应在压强恒定的密闭容器中进行,达平衡的时间变短 |
分析 由图象可知T1达到平衡用时较少,则T1>T2,而升高温度,CO2的物质的增多,说明升高温度平衡逆向移动,则正反应为放热反应,以此解答该题.
解答 解:A.由以上分析可知正反应为放热反应,故A错误;
B.T1>T2,反应为放热反应,升高温度平衡逆向移动,则平衡常数K1<K2,故B错误;
C.图中A点没有达到平衡,且二氧化碳的物质的量大于平衡状态,则正反应速率大于逆反应速率,反应应向平衡的方向进行,故C错误;
D.因反应物气体的物质的量大于生成物气体的物质的量,随着反应的进行,压强不断减小,上述反应在压强恒定的密闭容器中进行,应不断增大缩小体积,则达平衡的时间变短,故D正确.
故选D.
点评 本题考查物质的物质的量的平衡移动的图象等知识,为高考常见题型,题目难度中等,本题注意分析图象中二氧化碳的物质的量的变化,结合反应的特点判断外界条件对平衡移动的影响,试题培养了学生的分析、理解能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 适当升高温度能促进FeCl3水解 | |
| B. | 加水稀释能促进其水解,并提高Fe(OH)3的浓度 | |
| C. | 加少量浓盐酸能促进FeCl3水解 | |
| D. | 保存氯化铁溶液时应加入少量铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为加快漂白精的漂白速率,使用时可滴加几滴醋酸 | |
| B. | 在食品袋中放人盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 | |
| C. | 用含橙色酸性重铬酸钾的仪器检验酒驾,利用了乙醇的挥发性和还原性 | |
| D. | 光太阳能电池先将光能转化为化学能,然后再将化学能转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解和蛋白质水解都是由高分子化合物生成小分子物质的过程 | |
| B. | 乙烯分别使溴水和酸性KMnO4溶液褪色,反应原理相同 | |
| C. | C6H14有5种同分异构体 | |
| D. | CH4和Cl2按体积比1:3混合可制得纯净的CHCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 组别 | Ⅰ | Ⅱ |
| A | 常温下,乙烯和氯气混合 | 乙烷和氯气混合光照 |
| B | 乙酸、乙醇、浓硫酸混合,加热 | 在FeBr3催化下,苯与液溴反应 |
| C | 苯和浓硫酸、浓硝酸混合,加热到50~60℃ | 乙烯在一定条件下与水反应 |
| D | 由乙烯制取聚乙烯 | 蔗糖与稀硫酸混合,加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )
常温下,将除去表面氧化膜的A1、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示.反应过程中有红棕色气体产生.下列说法错误的是( )| A. | t1时刻前,A1片的电极反应为:2A1-6e-+3H2O═A12O3+6H+ | |
| B. | t1时,因A1在浓硝酸中钝化,氧化膜阻碍了A1继续反应 | |
| C. | t1之后,负极Cu失电子,电流方向发生改变 | |
| D. | 烧杯中发生的离子反应为:2NO2+2OH-═2NO3-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①是铝热反应 | B. | 反应②是置换反应 | C. | C2Cl6属于卤代烃 | D. | 氧化性:Al<Zn<C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属间发生置换反应 | |
| B. | 金属元素的最高价氧化物对应水化物的碱性强弱 | |
| C. | 1mol金属单质在反应中失去电子的多少 | |
| D. | 金属元素的单质与水或酸反应置换出氢气的难易 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 因SiO2不溶于水,故H2SiO3不是SiO2对应的酸,或者说SiO2不是H2SiO3的酸酐 | |
| B. | CO2通入Na2SiO3溶液中可以得到硅酸 | |
| C. | 因为高温时SiO2与Na2CO3反应生成CO2,故硅酸的酸性比碳酸强 | |
| D. | 硅的性质稳定,所以在自然界中可以以游离态存在 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com