
【题目】煤是“工业的粮食”,石油是“工业的血液”。有关煤和石油加工的说法正确的是
A. 煤的干馏产物主要是各类有机物
B. 石油的裂解、分馏和煤的干馏都属于化学变化
C. 煤焦油经过分馏可得到苯、甲苯等,说明煤中含有苯和甲苯
D. 石油的裂化,说明长链烃在高温条件下可以分解为短链烃
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】把一小块镁、铝合金放入6molL﹣l的NaOH溶液中,可以形成微型原电池.则该电池负极上发生的电极反应为( )
A.Mg﹣2e﹣═Mg2+
B.A1+4OH﹣﹣3e﹣═AlO2﹣+2H2O
C.4OH﹣﹣4e﹣═2H2O+O2↑
D.2H2O+2e﹣═2OH﹣+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在催化剂作用下,用乙醇制乙烯,乙醇转化率和乙烯选择性(生成乙烯的物质的量与乙醇转化的物质的量的比值)随温度、乙醇进料量(单位:mL·min-1)的关系如图所示(保持其他条件相同)。
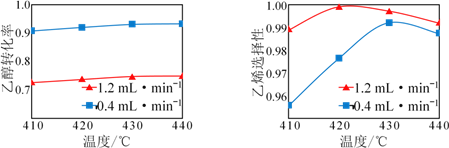
在410~440℃温度范围内,下列说法不正确的是
A. 温度一定时,随乙醇进料量增大,乙醇转化率减小
B. 温度一定时,随乙醇进料量增大,乙烯选择性增大
C. 乙醇进料量一定时,随温度的升高,乙烯选择性一定增大
D. 选择适当的催化剂在一定条件下,可大幅提高乙烯在最终产物中的比率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述与电化学腐蚀无关的是
A. 切过咸菜的菜刀不及时清洗易生锈
B. 线路连接时,有经验的电工从不把铝导线和铜导线接在一起
C. 银质奖章久置后表面逐渐变暗
D. 在轮船的尾部和船壳的水线以下,常装有一定数量的锌块
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五氧化二钒广泛用于冶金、化工等行业,主要用于冶炼钒铁.用作合金添加剂,占五氧化二钒总消耗量的80%以上,其次是用作有机化工的催化剂,为了增加V2O5的利用率,我们从废钒催化剂(主要成分V2O5,VOSO4,K2SO4,SiO2和Fe2O3等)中回收V2O5的一种生产工艺流程示意图如下:
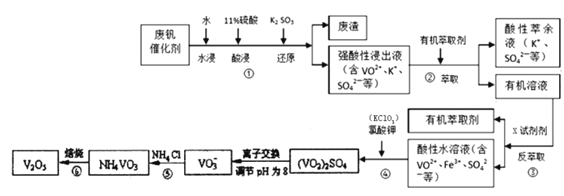
部分含钒物质在水中的溶解性如下,回答下列问题:
物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
溶解牲 | 可溶 | 难溶 | 难溶 | 易溶 |
(l)①中废渣的主要成分是____;①中V2O5发生反应的离子方程式为_____________。
(2)②,③中的变化过程可简化为(下式中的R表示VO2+或Fe3+,HA表示有机萃取剂的主要成分):R2(SO4)n(水层)+2nHA(有机层)![]() 2RA(有机层)+nH2SO4(水层)。②中萃取时必须加入适量碱,其原因是________________;实验室进行萃取操作主要使用的玻璃仪器为________________。
2RA(有机层)+nH2SO4(水层)。②中萃取时必须加入适量碱,其原因是________________;实验室进行萃取操作主要使用的玻璃仪器为________________。
(3)实验室用的原料中V2O5占6%(原料中的所有钒已换算成V2O5)。取l00g该废钒催化剂按工业生产的步骤进行实验,当加入100 mL0.1mol/L的KC1O3溶液时,溶液中的钒恰好被完全处理,假设以后各步钒没有损失,则该实验中钒的回收率是____(己知V2O5的相对分子质量为182)。
(4) 25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间的关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.6 | 96.4 | 93.1 | 89.3 |
试判断在实际生产时,⑤中加入氨水调节溶液的最佳pH为_________;若钒沉淀率为93.1%时不产生Fe( OH)3沉淀,则此时溶液中c(Fe3+)=_________。(已知:25℃时k[Fe(OH)3]=2.6×l0-39.)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3 , 还含有Fe2O3、SiO2)提取氧化铝,冶炼铝的原料,提取的操作过程如图: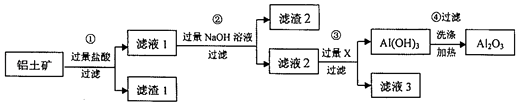
请回答下列问题:
(1)写出步骤①中发生反应的离子方程式;滤渣①的成分为 .
(2)写出步骤②中生成含铝化合物的化学方程式;能否将此步骤中的NaOH 溶液更换为氨水?(填“能”或“不能”).若不能,请说明理由:(若能,则此空不答).
(3)步骤③中的X 为(填化学式),发生反应的离子方程式为 .
(4)若铝土矿的质量为mkg,最后得到A12O3的质量为nkg(忽略提取过程中铝元素的损失),则铝土矿中铝元素的质量分数为(用含m、n 的代数式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色溶液中,下列离子能大量共存的是
A. Fe2+、Na+、SO42-、Cl-
B. Na+、Ba2+、CO32-、NO3-
C. Cu2+、K+、Cl-、SO42-
D. K+、Na+、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,在一固定容积的密闭容器中发生反应:A(g)+B(g)![]() C(s)△H<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
C(s)△H<0,按照不同配比充入A、B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
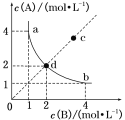
A. T℃时,该反应的平衡常数值为4
B. c点没有达到平衡,此时反应向逆向进行
C. 若c点为平衡点,则此时容器内的温度高于T℃
D. T℃时,直线cd上的点均为平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH3COOOH(过氧乙酸)广泛应用于环境和医院手术室的消毒,某校化学兴趣小组想利用CH3COOH+H2O2=CH3COOOH+H2O来制取过氧乙酸,查得相关数据如下:
物质 | 沸点 ℃ | 熔点 ℃ | 溶解性 |
CH3COOH | 117.9 | 16.6 | 能溶于水及酒精等有机溶剂 |
H2O2 | 150.2 | -0.43 | 溶于水及酒精 |
CH3COOOH | 105 | 0.1 | 溶于水及酒精等有机溶剂 |
同时查得过氧乙酸具有:刺激性气味,易燃;加热至100℃即猛烈分解;遇火或受热、受震都可引起爆炸;对金属具有较强的腐蚀性。回答以下问题:
(1)利用如图装置进行制取,实验中水浴温度应控制在________100℃(填“>”或“<”或“=”),原因是:____________________________________________________________

(2)为了使实验顺利进行,B处应接一个_________(填一种装置),然后缓慢打开图中开关通入空气,从而得到过氧乙酸溶液。
(3)实验结束后得到一定量的过氧乙酸,利用如下反应测定该产物的纯度:
2KMnO4+5H2O2 +3H2SO4=K2SO4+2MnSO4+8H2O+5O2↑
2KI+ CH3COOOH+2 H2SO4=2KHSO4+I2+ CH3COOH+H2O
I2+2Na2S2O3=2NaI+Na2S4O6
①取10.00mL制得的过氧乙酸溶液,加水稀释到1000mL,用移液管取20.00mL至锥形瓶中,加入足量稀硫酸酸化后,再用____________(填“酸式滴定管”或“碱式滴定管”)装0.100mol/L的KMnO4溶液进行滴定至_______________________________________现象时恰好完全反应,从而将混在过氧乙酸中的H2O2除去。然后再加入过量KI溶液,加入几滴淀粉,再用0.100mol/L的Na2S2O3滴定消耗了12.00mL。一般工业制得的过氧乙酸质量分数为18% ~ 23%。如果测得实验室制得的过氧乙酸溶液密度为1.15gcm-3。试通过计算判断该溶液是否合格_____________。
②滴定过程中,下列操作会使结果偏大的是_________。
A.滴加Na2S2O3时开始平视滴定管,结束时俯视滴定管。
B.装标准Na2S2O3溶液的滴定管未用标准Na2S2O3溶液润洗。
C.移液管在使用之前未用烘干,里面附着水珠就用来量取待测液
D. .滴加Na2S2O3时开始仰视滴定管,结束时平视滴定管。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com