
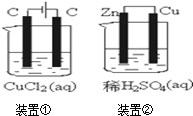
| A. | 两个装置中都发生了化学变化,都由化学能转变为电能 | |
| B. | 装置②中电流方向是从Zn经导线流入Cu | |
| C. | 反应开始阶段,两个装置中均有氢气产生 | |
| D. | 电极反应式:阳极2Cl--2e-→Cl2↑正极2H++2e-→H2↑ |
分析 ①是电解池②是原电池,①中阳极上氯离子放电生成氯气,阴极上铜离子放电生成铜,②中锌作负极,铜作正极,负极上锌失电子发生氧化反应,正极上氢离子得电子发生还原反应,电流从正极沿导线流向负极,以此解答该题.
解答 解:A.①是电解池,是电能转化为化学能的装置,②是原电池,是化学能转化为电能的装置,故A错误;
B.②中电流的方向是从铜沿导线流向锌,故B错误;
C.反应开始阶段,①中阳极上析出氯气,阴极上析出铜,②中正极上生成氢气,负极上生成锌离子,故C错误;
D.阳极上失电子发生氧化反应,正极上得电子发生还原反应,其电极反应式:①中阳极 2Cl--2e→Cl2↑②中正极 2H++2e→H2↑,故D正确;
故选D.
点评 本题考查原电池和电解池原理,为高频考点,侧重于学生的分析能力的考查,注意把握原电池、电解池的工作原理,把握原电池和电解池的区别,难度不大.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:选择题
| A. | 碘酒是指碘单质的乙醇溶液 | |
| B. | 浓硫酸可以刻蚀石英制艺术品 | |
| C. | 84消毒液的有效成分是NaClO | |
| D. | 氢氧化铝、小苏打等可用于治疗胃酸过多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCl | B. | CH3C(CH3)2Br | C. | (CH3)3CCOOCH(CH3)2 | D. | CH3C(CH3)2CH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
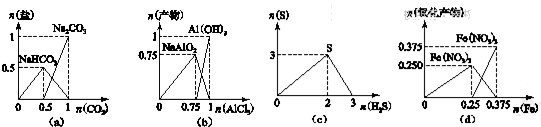
| A. | 图(a):n(NaOH)═1 mol时,CO2和NaOH溶液反应生成的盐 | |
| B. | 图(b):n(NaOH)═3 mol时,AlCl3溶液和NaOH 溶液反应的产物 | |
| C. | 图(c):n(H2S)+n(SO2)═3 mol时,H2S与SO2反应生成的S | |
| D. | 图(d):n(HNO3)═1 mol时,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑦⑧⑨⑩ | B. | ①②③⑤⑧⑨ | C. | ②⑤⑥⑦⑧ | D. | ②④⑦⑧⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向豆浆中加入石膏制得可口的豆腐 | |
| B. | 蒸发饱和食盐水析出氯化钠晶体 | |
| C. | 向沸水中逐滴加入饱和的FeCl3溶液,得到红褐色透明的分散系 | |
| D. | 氢氧化铁溶胶、淀粉溶液、云雾等均具有丁达尔现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com