
将0.2mol两种气态烃组成的混合气体完全燃烧后得到(标准状况下)6.72L二氧化碳和7.2g水, 下列说法正确的是( )
A.一定有乙烯 B.可能有乙烯 C.一定没有甲烷 D.可能有乙烷
科目:高中化学 来源: 题型:
下列对物质用途的描述中,错误的是( )
A.铝可用于冶炼某些熔点较高的金属
B.Na2O2可用作漂白剂
C.碱石灰可用于干燥CO2、O2等气体
D.小苏打可用于治疗胃酸过多
查看答案和解析>>
科目:高中化学 来源: 题型:
某种激光染料,应用于可调谐染料激光器,它由C、H、O三种元素组成,分子球棍模型如图所示,下列有关叙述不正确的是( )
A.1 mol该物质完全燃烧最多能消耗10.5mol 的氧气
B.能使酸性KMnO4溶液褪色
C.1 mol该物质最多能与4 mol H2加成
D.分子式为C10H9O3
查看答案和解析>>
科目:高中化学 来源: 题型:
元素周期表是一座开放的“元素大厦”,元素大厦尚未充满。若发现119号元素,请您在元素大厦中安排好它的“房间” ( )
A.第七周期第0族 B.第六周期ⅡA族 C.第八周期第ⅠA族 D.第七周期第ⅦA族
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z、M 、N按原子序数依次递增的五种短周期元素,其中Z、M、N同周期,X、 Z同主族且X是原子半径最小的原子;Y、N同主族,Z+与Y2—具有相同的电子层结构;M的单质晶体熔点高、硬度大,是一种重要的半导体材料。
(1)M的元素名称 ,N在元素周期表中的位置 。
(2)离子半径比较:r(Z+) r(Y2—)。(填“>”、“=”或“<”)
(3)X与Z形成的化合物A是 (填“离子化合物”或“共价化合物”),A与X2Y反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.活化分子间所发生的碰撞为有效碰撞
B.增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大的主要原因是增加了单位体积内活化分子的百分数
D.有气体参与的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子总数,从而使反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
已知次氯酸是比碳酸还弱的酸,反应Cl2 + H2O 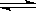 HCl + HClO达平衡后,要使HClO浓度增大,可加入( )
HCl + HClO达平衡后,要使HClO浓度增大,可加入( )
A.6mol/L NaOH溶液 B.6mol/L H2SO4溶液
C.CH3COONa固体 D.Na2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在10L容器中,加入2mol的SO2(g)和2mol的NO2(g),保持温度恒定,发生反应:
SO2(g)+ NO2(g) 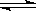 SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。当达到平衡状态时,测得容器中SO2(g)的转化率为50%。
试求:该温度下、该容器中,再继续加入1mol的SO2(g),则:
(1)化学平衡将向________方向移动,NO2的转化率将____________;
(2)经计算,当达到新的平衡状态时,容器中SO2(g)的浓度是_______mol/L;
(3)整个过程中,SO2的转化率由50%变为_______%,NO2的转化率由__________%变为_______%。
(4)计算结果给我们的启示是:增大一种反应物物的用量,其转化率将________________(填“增大” 、“不变”或“减小”)另一反应物的转化率将____________(填“增大” 、“不变”或“减小”)。现实生产中的意义是:可以通过增大________的用量,来提高成本高的反应物的利用率。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com