

| A. | 3种单体通过缩聚反应聚合 | B. | 形成该化合物的单体只有2种 | ||
| C. | 其中一种单体为 | D. | 其中一种单体为1,5-二甲基苯酚 |
分析 加聚反应是由不饱和单体(如碳碳双键,碳碳叁键以及碳氧双键等)聚合高分子的反应,其产物只有一种高分子化合物;缩聚反应是一类有机化学反应,是具有两个或两个以上官能团的单体,相互反应生成高分子化合物,同时产生有简单分子(如 H2O、HX、醇等)的化学反应;
由高聚物的结构简式可知,连接主链中含有肽键,为缩聚反应生成高聚物,据此判断其单体.
解答 解:观察本题中高分子化合物的,首先会联想到酚醛树脂的结构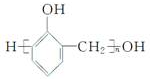 ,它对应的单体是
,它对应的单体是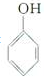 和HCHO.将题给有机物的结构再与酚醛树脂的结构比较,多出部分必然要用到的单体
和HCHO.将题给有机物的结构再与酚醛树脂的结构比较,多出部分必然要用到的单体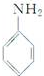 .由此可知,本题高分子合成时所用到的单体有
.由此可知,本题高分子合成时所用到的单体有 、HCHO和
、HCHO和 ,这三种单体发生聚合时应为缩聚反应.
,这三种单体发生聚合时应为缩聚反应.
故选AC.
点评 本题考查缩聚反应生成高聚物的单体的判断方法,要求学生具有分析和解决问题的能力,难度中等.


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:解答题
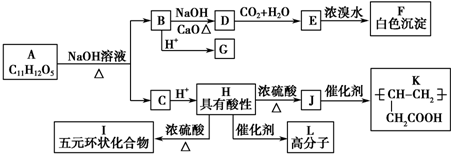
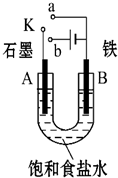 某课外活动小组用如图装置进行实验,试回答下列问题.
某课外活动小组用如图装置进行实验,试回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
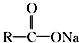 +NaOH$→_{△}^{CaO}$R═H+Na2CO3
+NaOH$→_{△}^{CaO}$R═H+Na2CO3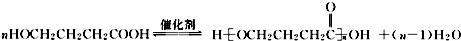 .
. .
.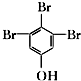 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | ||
| X | T | Z |
| Q |
| A. | X的最高价氧化物能溶于强碱 | B. | 非金属性:T>R | ||
| C. | 单质导电性:Z>T>X | D. | R与Q的原子核外电子数相差16 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
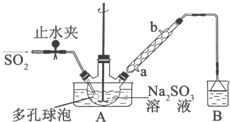 次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解.在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解.在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
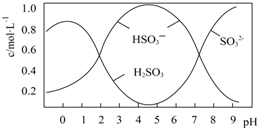 葡萄酒常用Na2S2O5做抗氧化剂.
葡萄酒常用Na2S2O5做抗氧化剂.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/s | 0 | 5 | 15 | 25 | 35 |
| N(M)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A. | 35s时,N的浓度为0.80mol•L-1 | |
| B. | 达到平衡时,M的转化率为80% | |
| C. | 相同温度下若起始时向容器中充入1.0molP,则达到平衡时P的浓度为0.1mol•L-1 | |
| D. | 相同温度下,起始时向容器中充入0.20molM、0.20molN和1.0molP,反应达到平衡前v(逆)<v(正) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com