
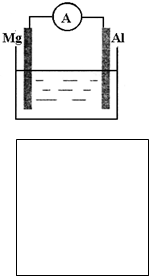
 (1)如图所示装置:①若烧杯中溶液为稀硫酸,则观察到的现象为
(1)如图所示装置:①若烧杯中溶液为稀硫酸,则观察到的现象为


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
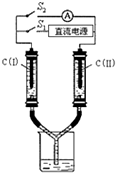 电化学在工业生产中有广泛应用.
电化学在工业生产中有广泛应用.
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 | 3 |
查看答案和解析>>
科目:高中化学 来源:2011届湖南省浏阳一中高三上学期第五次月考化学试卷 题型:填空题
实验室用下列方法测定某水样中O2的含量。
(1)用如图所示装置,使水中溶解的O2在碱性条件下将Mn2+氧化成MnO(OH)2的反应的离子方程式为______________________________________。
实验步骤:
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是______________________________________。
②用注射器抽取20.00 mL某水样从A处注入锥形瓶。
③再分别从A处注入含m mol NaOH的溶液及过量的MnSO4溶液。
④完成上述操作后,下面应进行的操作是_______________。c是长橡胶管,使用较长橡胶管的目的是__________________________________。
(2)用I-将生成的MnO(OH)2再还原为Mn2+,反应的离子方程式为MnO(OH)2+2I-+4H+===Mn2++I2+3H2O。
实验步骤:
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸溶液。
⑥重复④的操作。
(3)用Na2S2O3标准溶液滴定步骤(2)中生成的I2,反应的化学方程式为I2+2Na2S2O3===2NaI+Na2S4O6。
实验步骤:
⑦取下锥形瓶,向其中加入2~3滴__________作指示剂。
⑧用0.005 mol·L-1的Na2S2O3滴定至终点。
(4)计算。滴定过程中,滴定前后滴定管中的液面读数如图所示。
⑨经计算,此水样中氧(O2)的含量为________mg·L-1。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖南省高三上学期第五次月考化学试卷 题型:填空题
实验室用下列方法测定某水样中O2的含量。

(1)用如图所示装置,使水中溶解的O2在碱性条件下将Mn2+氧化成MnO(OH)2的反应的离子方程式为______________________________________。
实验步骤:
①打开止水夹a和b,从A处向装置内鼓入过量N2,此操作的目的是______________________________________。
②用注射器抽取20.00 mL某水样从A处注入锥形瓶。
③再分别从A处注入含m mol NaOH的溶液及过量的MnSO4溶液。
④完成上述操作后,下面应进行的操作是_______________。c是长橡胶管,使用较长橡胶管的目的是__________________________________。
(2)用I-将生成的MnO(OH)2再还原为Mn2+,反应的离子方程式为MnO(OH)2+2I-+4H+===Mn2++I2+3H2O。
实验步骤:
⑤打开止水夹a、b,分别从A处注入足量NaI溶液及含n mol H2SO4的硫酸溶液。
⑥重复④的操作。
(3)用Na2S2O3标准溶液滴定步骤(2)中生成的I2,反应的化学方程式为I2+2Na2S2O3===2NaI+Na2S4O6。
实验步骤:
⑦取下锥形瓶,向其中加入2~3滴__________作指示剂。
⑧用0.005 mol·L-1的Na2S2O3滴定至终点。
(4)计算。滴定过程中,滴定前后滴定管中的液面读数如图所示。

⑨经计算,此水样中氧(O2)的含量为________mg·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com