
【题目】设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是
A. 1mol NH3所含有的原子数为NA
B. 常温常压下,22.4L氧气所含的原子数为2NA
C. 常温常压下,48g O3所含的氧原子数为3NA
D. 1 L 0.1mol/LNaCl溶液中所含的Na+为NA
科目:高中化学 来源: 题型:
【题目】CaCO3与稀盐酸反应生成CO2的量与反应时间的关系如图所示。下列结论不正确的是
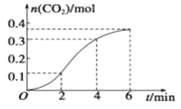
A. 反应在2~4 min内平均反应速率最大
B. 反应开始4 min内温度比浓度对反应速率的影响大
C. 4 min后,反应速率减小的主要原因是c(H+)减小
D. 反应在2~4 min内生成CO2的平均反应速率为v(CO2)=0.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:[CoCl4]2-(蓝色)与[Co(H2O)6]2+(粉红色)之间存在如下平衡:[CoCl4]2-+6H2O [Co(H2O)6]2++4Cl- △H<0。现有呈现紫色的氯化钴溶液。
(1)甲同学向上述溶液中通入HC1,发现溶液变为___色;
(2)乙同学向上述溶液中加水,平衡___(填“向右”、“向左”或“不”)移动。为使平衡保持该移动方向,还可采取的措施有____(写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,不属于取代反应的是( )
A. CH3Cl+Cl2![]() CH2Cl2+HCl
CH2Cl2+HCl
B. CH4+2O2![]() CO2+H2O
CO2+H2O
C. CH3CH2Br +H2O→CH3CH2OH + HBr
D. CH3CH3+Cl2![]() C2H5Cl+HCl
C2H5Cl+HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化工厂为了综合利用生产过程中的副产品CaSO4,与相邻的合成氨厂联合设计了以下制备(NH4)22SO4的工艺流程:
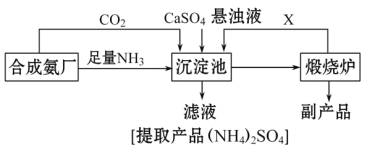
请回答以下问题:
(1)工业合成氨反应的条件是_____________________。沉淀池中发生的主要反应方程式是________________________。该反应能够发生的原因是__________________________。
(2)提纯滤液以获得(NH4)2SO4晶体,必要的操作步骤是:__________(填序号)。
A.萃取 B.蒸发浓缩 C.冷却结晶 D.蒸馏
(3)上述生产流程中,有关NH3的作用及说明正确的是:__________(填序号)。
A.提供制备所需的氮元素
B.增大CO32-的浓度促进反应发生
C.作反应的催化剂
D.生产1 mol (NH4)2SO4,至少消耗2 mol NH3
(4)该生产过程中的副产品是_______________,从绿色化学和资源综合利用的角度说明上述流程的主要优点是______________.缺点是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题。(B中装的是无水硫酸铜)

(1)A是氯气发生装置,实验室制取Cl2的原理是_____(用离子方程式表示)
(2)该实验中A部分的装置是_____(填字母)
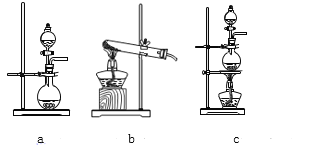
(3)若用含有0.2molHCl的浓盐酸与足量的氧化剂反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是(填序号)_____
A.浓盐酸的浓度随着反应的进行变稀以后,将不再反应
B.加热时浓盐酸因挥发而损失
C.氧化剂不足
(4)装置E的作用是______。
(5)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,乙同学提出在某两个装置之间再加一个装置。该装置中应放入_______试剂。
(6)用如图所示装置,收集一试管甲烷和氯气的混合气体,光照后观察到量筒内形成一段水柱,认为有氯化氢生成。
①该反应的反应类型为_________;
②该反应的化学方程式为________;(只写第一步)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍。电池总反应为:C2H5OH +3O2= 2CO2 +3H2O,电池示意图如下图。下面对这种电池的说法正确的是:
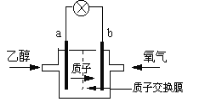
A. 标准状况下,通入5.6LO2并完全反应后,有0.5mol电子转移
B. 电池工作时电子由b极沿导线经灯泡再到a极
C. 电池正极的电极反应为:4H+ +O2 +4e- =2H2O
D. b极为电池的负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-—选修3:物质结构与性质]东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的成键原子是_____。
③氨的沸点(填“高于”或“低于”)膦(PH3),原因是______;氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。
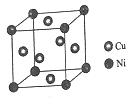
①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生探究0.25mol/L Al2( SO4)3溶液与0.5mol/L Na2CO3溶液的反应,实验如下:
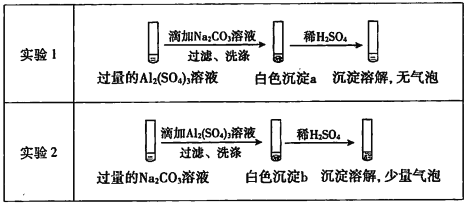
下列分析不正确的是
A. 实验I中,白色沉淀a是Al(OH)3
B. 实验2中,白色沉淀b含有CO32-
C. 实验l、2中,白色沉淀成分不同的原因与混合后溶液的pH无关
D. 检验白色沉淀a、b足否洗涤干净,均可用盐酸酸化的BaCl2溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com