
【题目】实验室用Ca与H2反应制取氢化钙(CaH2)。下列实验装置和原理不能达到实验目的的是( )
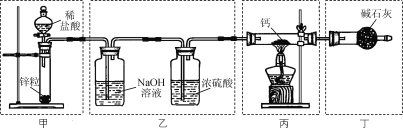
A. 装置甲制取H2B. 装置乙净化干燥H2
C. 装置丙制取CaH2D. 装置丁吸收尾气
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】含铬(Ⅵ)废水能诱发致癌,对人类和自然环境有严重的破坏作用。利用Cu2O光催化可以处理含有Cr2O72-的废水。
Ⅰ.制取Cu2O
(1)电解法:利用铜和钛做电极,电解含有NaCl和NaOH的溶液时,反应只消耗了铜和水,体系pH及Cl-浓度维持不变(溶液体积变化忽略不计)。阳极电极反应式是_______。
(2)还原法:控制100℃、pH=5的条件时,利用亚硫酸钠与硫酸铜溶液反应可以制得Cu2O,同时产生SO2气体。反应过程中需要不断地加入烧碱,其原因是_______。
Ⅱ.利用Cu2O光催化处理含Cr2O72-的废水的研究。
(1)光照射到Cu2O光催化剂上产生光催化反应,Cr2O72-和H2O分别在光催化反应中形成的微电极上发生电极反应,反应原理如图所示。写出Cr2O72-转化Cr3+的电极反应:_______。
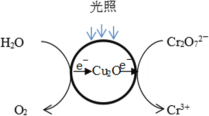
(2)研究中对Cu2O的作用提出两种假设:
a.Cu2O作光催化剂;b.Cu2O与Cr2O72-发生氧化还原反应。
已知:Cu2O的添加量是2×10-4mol/L,Cr2O72-的初始浓度是1×10-3mol/L;对比实验(pH=3.0且其他条件相同),反应1.5小时结果如图所示。结合试剂用量数据和实验结果可得到的结论是_______,依据是_______。

(3)溶液的pH对Cr2O72-降解率的影响如图所示。
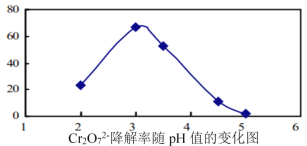
已知:Cu2O![]() Cu+CuSO4;酸性越大,Cr2O72-被还原率越大。
Cu+CuSO4;酸性越大,Cr2O72-被还原率越大。
①pH分别为2、3、4时,Cr2O72-的降解率最好的是___________,其原因是___________。
②已知pH=5时,会产生Cr(OH)3沉淀。pH=5时,Cr2O72-的降解率低的原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图,回答问题。
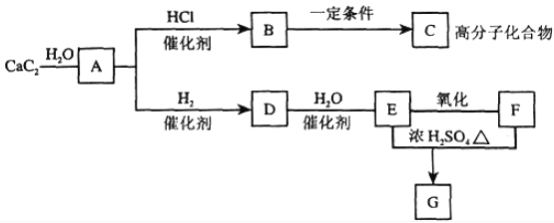
(1)有机物C的结构简式:________。
(2)①反应DE的化学方程式是_____________。
②E和F反应生成G的化学方程式是__________,反应类型为_________。
③实验室制取A的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:氧化锂(Li2O)晶体形成过程中的能量变化如图所示
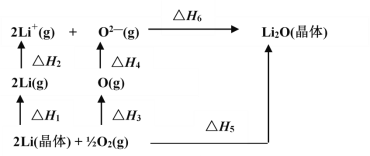
下列说法正确的是
A. △H1< 0,△H2>0B. -△H5 +△H1 +△H1 +△H3+△H4 +△H6 =0
C. △H3<0,△H4 < 0D. △H1+ △H2+△H3 +△H4 =△H5+△H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铂、钴、镍及其化合物在工业和医药等领域有重要应用。回答下列问题:
(1)筑波材料科学国家实验室科研小组发现了在5K下呈现超导性的晶体CoO2,该晶体具有层状结构。
①晶体中原子Co与O的配位数之比为_________。
②基态钴原子的价电子排布图为_______。
(2)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于_____晶体;写出两种与CO具有相同空间构型和键合形式的分子或离子:_______。
(3)某镍配合物结构如图所示:
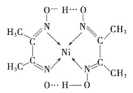
①分子内含有的化学键有___________(填序号).
A 氢键 B 离子键 C 共价键 D 金属键 E 配位键
②配合物中C、N、O三种元素原子的第一电离能由大到小的顺序是N> O>C,试从原子结构解释为什么同周期元素原子的第一电离能N>O_________。
(4)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属" ,其结构如图所示。

①"分子金属"可以导电,是因为______能沿着其中的金属原子链流动。
②"分子金属"中,铂原子是否以sp3的方式杂化?_________(填“是"或“否"),其理由是__________。
(5)金属铂晶体中,铂原子的配位数为12,其立方晶胞沿x、y或z轴的投影图如图所示,若金属铂的密度为d g·cm-3,则晶胞参数a=_______nm(列计算式)。
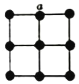
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向某浓度的二元弱酸H2C2O4溶液中逐滴加入NaOH溶液,pC与溶液pH的变化关系如图所示(pC=-lgx,x表示溶液中溶质微粒的物质的量浓度)。下列说法正确的是
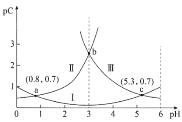
A.常温下,H2C2O4的Ka1=100.8
B.pH=3时,溶液中![]()
C.pH由0.8增大到5.3的过程中,水的电离程度逐渐增大
D.常温下,随着pH的增大,![]() 的值先增大后减小
的值先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物苯:常常作为工农业生产中的良好溶剂。
(1)若将苯倒入盛有碘水的试管中,振荡后静置,现象是__________________________,说明苯的密度比水_________,且________________。
(2)若将乒乓球碎片、食盐固体分别加入盛有苯的试管中,振荡后静置,现象是___________________,说明苯是很好的_____________________________。
(3)将盛有苯的两支试管分别插入100℃的沸水和0℃的冰水的现象是________________________,说明苯的沸点_________________,熔点_________。
人们对苯的认识有一个不断深化的过程。
(4)由于苯的含碳量与乙炔相同,人们认为它是一种不饱和烃,写出分子式为C6H6的一种含两个三键且无支链的链烃的结构简式_____________________________________。
(5)已知分子式为C6H6的有机物有多种,其中的两种为:
(I)![]() (II)
(II)![]() 这两种结构的区别表现在以下两方面:
这两种结构的区别表现在以下两方面:
①定性方面(即化学性质方面):(II)能___________(填字母),而(I)不能。
a. 被高锰酸钾酸性溶液氧化 b. 与溴水发生取代反应
c. 与溴发生取代反应 d. 与氢气发生加成反应
②定量方面(即消耗反应物的量的方面):1molC6H6与H2加成时:(I)需要H2______mol,而(II)需要H2_____mol。
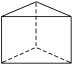
(6)今发现C6H6还可能有另一种如右图所示的立体结构,该结构的一氯代物有_________种;现代化学认为苯分子中碳碳之间的键是_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸镍是电镀工业必不可少的化工原料。从不锈钢废渣(主要含Fe42.35%、Cr9.67%、Ni5.1%、C4.7%、Si3.39%等)中制取硫酸镍晶体的工艺流程如图:
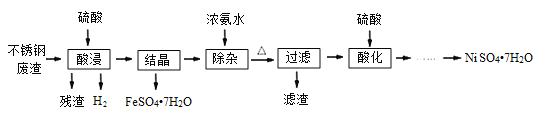 已知:①Cr3+与氨水反应时有少量Cr3+生成[Cr(NH3)6]3+,但加热时该络合物易分解。Ni2+与氨水反应生成[Ni(NH3)6]2+,该络合物加热时稳定,用硫酸酸化时生成相应的硫酸盐。
已知:①Cr3+与氨水反应时有少量Cr3+生成[Cr(NH3)6]3+,但加热时该络合物易分解。Ni2+与氨水反应生成[Ni(NH3)6]2+,该络合物加热时稳定,用硫酸酸化时生成相应的硫酸盐。
②Na2CrO4溶液中加酸调节pH为3.5时,CrO42-转化为Cr2O72-。
③相关物质在不同温度时溶解度如下表:
温度 溶解度/g 物质 | 20℃ | 30℃ | 40℃ | 60℃ | 80℃ | 90℃ |
Na2SO4 | 19.5 | 40.8 | 48.8 | 45.3 | 43.7 | 42.7 |
Na2Cr2O7 | 183 | 198 | 215 | 269 | 376 | 405 |
(1)“酸浸”后得到的溶液中主要含有FeSO4、NiSO4、Cr2(SO4)3,生成NiSO4的化学方程式为___。“酸浸”时需控制温度为90℃左右,可以采用的加热方式是___。
(2)“过滤”前,适当加热的目的是___。
(3)对“过滤”所得的滤渣进行洗涤,检验滤渣已洗涤干净的方法是___。
(4)“过滤”时产生的滤渣可用于制备Na2Cr2O7晶体。
①滤渣经干燥后与Na2CO3混合在空气中煅烧生成Na2CrO4和CO2,此反应的化学方程式为___。
②请补充完整上述煅烧后混合物制备Na2Cr2O7晶体(橙红色)的实验方案:水浸,过滤,___,烘干得Na2Cr2O7晶体(必须使用的试剂有:硫酸,蒸馏水)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知原子序数,可能推断原子的
①质子数 ②中子数 ③质量数 ④核电荷数 ⑤核外电子数
⑥原子结构示意图 ⑦元素在周期表中的位置
A. ①②③④⑥ B. ①④⑤⑥⑦
C. ②③④⑤⑦ D. ③④⑤⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com