
 +H2O2
+H2O2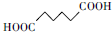 +H2O
+H2O
分析 以环己酮为原料在钨酸钠催化下,利用双氧水氧化可得到己二酸,涉及制备、分离提纯及产品分析,并对流程中操作的注意点及操作方法进行了讨论,可结合产品的性质,反应混合物的组成进行分析解答;
(1)只有饱和溶液里才有晶体析出,故步骤③从溶液里析出晶体时中析出不多,可考虑对反应混合液进行浓缩,促进晶体析出;
(2)当混合液里有多种溶质时可结合溶解度的差异进行重结晶,并选择趁热过滤,减少其它固体溶质析出,类似于用重结晶分离KNO3中混合有少量KCl;
(3)结合常见仪器可知仪器a为布氏漏斗,装置B为安全装置,可防倒吸,连接自来水可通过水流进行抽压,利于B装置的抽滤分离,可按正常操作顺序排序;
(4)滴定终点的分析可借助酚酞在己二酸溶液里的颜色与在氢氧化钠溶液里的颜色来分析,根据酸碱中和反应的原理,结合消耗的NaOH溶液的物质的量计算样品中含有的己二酸的物质的量,再计算纯度.
解答 解:(1)若步骤③中固体析出不多,应采取的操作为将溶液加热浓缩至25~30 mL,再冷却使晶体析出,故答案为:将溶液加热浓缩至25~30 mL,再冷却结晶;
(2)重结晶过程中的趁热过滤操作除去了不溶性杂质,故答案为:趁热过滤;
(3)仪器a的名称为布氏漏斗;装置B的作用是防止发生倒吸;装置C接在水龙头上起抽气作用,使吸滤瓶、安全瓶中的压强减小;减压过滤的正确操作顺序为②③①⑤④,故答案为:布氏漏斗;防止发生倒吸;抽气,使吸滤瓶、安全瓶中的压强减小;②③①⑤④;
(4)用0.1 mol•L-1的NaOH标准溶液滴定至终点时溶液颜色由无色变为浅红色,并在半分钟内不褪色;滴定时消耗NaOH溶液的体积为18.50-2.50=16.00(mL),NaOH的物质的量为0.1mol/L×0.016L=0.0016mol,己二酸的物质的量为0.0016mol÷2=0.0008mol,样品中己二酸的质量分数=$\frac{0.0008mol×146g/mol}{0.12g}$×100%=97.3%,故答案为:无色;浅红色;97.3%.
点评 本题利用氧化还反应原理进行物质制备,涉及混合物的分离提纯及纯度分析,综合性较强,通过练习对学生解题能力的培养有一定帮助,属中等难度.


 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案科目:高中化学 来源: 题型:选择题
| A. | 4:1 | B. | 1:4 | C. | 3:1 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .写出B的试管中所发生反应的化学方程式HBr+AgNO3=AgBr↓+HNO3.
.写出B的试管中所发生反应的化学方程式HBr+AgNO3=AgBr↓+HNO3.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 开始沉淀 | 沉淀完全 | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 容器 | 反应物投入的量 | 反应物的 转化率 | CH3OH的浓度 | 能量变化 (Q1、Q2、Q3均大于0) |
| 甲 | 1mol CO和2mol H2 | α1 | c1 | 放出Q1kJ热量 |
| 乙 | 1mol CH3OH | α2 | c2 | 吸收Q2kJ热量 |
| 丙 | 2mol CO和4mol H2 | α3 | c3 | 放出Q3kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ① | HF | Ka=6.8×10-4 mol•L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol•L-1 |
| ③ | HCN | Ka=6.2×10-10 mol•L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7 mol•L-1 Ka2=4.7×10-11 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +
+ $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$ +H2O
+H2O| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 异戊醇 | 88 | 0.8123 | 131 | 微溶 |
| 乙酸 | 60 | 1.0492 | 118 | 溶 |
| 乙酸异戊酯 | 130 | 0.8670 | 142 | 难溶 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com