
某可逆反应L(s)+G(g)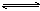 3R(g) △H>0,右图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示
3R(g) △H>0,右图表示外界条件温度、压强的变化对上述反应的影响。试判断图中y轴可以表示
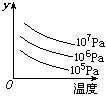 A.平衡混合气中R的质量分数 B.达到平衡时G的转化率
A.平衡混合气中R的质量分数 B.达到平衡时G的转化率
C.平衡混合气中G的质量分数 D.达到平衡时L的转化率
 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案科目:高中化学 来源: 题型:
在CuCl2水溶液中存在如下平衡:2++4Cl- 2-+4H2O能使黄绿
(蓝) (绿)
色CuCl2溶液向蓝色转化的操作是
A、蒸发浓缩 B、加水稀释 C、加入AgNO3 D、加入食盐晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
在固定体积的密闭容器中加入4mol A和2mol B发生如下反应2A(g)+B(g) 3C(g)+D(g)达到平衡时C的浓度为m mol/L,若温度不变时按下列4种配比作为起始物质,达到平衡后C浓度仍为m mol/L的是
3C(g)+D(g)达到平衡时C的浓度为m mol/L,若温度不变时按下列4种配比作为起始物质,达到平衡后C浓度仍为m mol/L的是
A.2molA+1molB B.2molA+1molB+3molC+1mol D
C.3molC+1molD D.4molA+2molB+3molC
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式中,正确的是
A.BaSO4 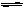 Ba2+ + SO42- B.2H2O
Ba2+ + SO42- B.2H2O 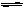 H3O+ + OH-
H3O+ + OH-
C.NaHCO3 = Na ++ H+ + CO32- D.NH3•H2O = NH4+ + OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,对于密闭容器中进行的可逆反应:2HI(g) 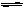 H2(g)+I2(g),下列说法中,能说明这一反应已达到化学平衡状态的是
H2(g)+I2(g),下列说法中,能说明这一反应已达到化学平衡状态的是
A.正、逆反应速率都等于零 B.HI、H2、I2的浓度相等
C.HI、H2、I2在容器中共存 D.HI、H2、I2的浓度均不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达平衡,平衡常数K=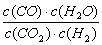 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A.该反应的焓变为正值 B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小 D. 该反应化学方程式为CO+H2O CO2+H2
CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,反应N2(g)+3H2(g) 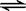 2NH3(g ) 在10L的密闭容器中进行,
2NH3(g ) 在10L的密闭容器中进行,
(1)测得2min内,N2的物质的量由20mol减小到8mol,则2min内H2的反应速率为_____。
(2)当该反应达到化学平衡时,则其平衡常数表达式为 ,如果此时向容器中增加氮气,那么氢气的转化率会 (填增大或降低)。
(3)生成物氨气能与水反应,生成的一水合氨属于 (填强电解质或弱电解质)。
(4)在含有酚酞的0.1 mol / L氨水中加少量的 NH4Cl晶体,则溶液颜色____(填字母)。
A.变蓝色 B.变深 C.变浅 D.不变
(5)工业合成氨的反应为N2(g)+3H2(g)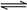 2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为
2NH3(g)。设在容积为2.0 L的密闭容器中充入0.60 mol N2(g)和1.60 mol H2(g),反应在一定条件下达到平衡时,NH3的物质的量分数(NH3的物质的量与反应体系中总的物质的量之比)为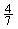 。求(写出计算过程)
。求(写出计算过程)
① 该条件下N2的平衡转化率;
② 该条件下反应2NH3(g)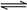 N2(g)+3H2(g)的平衡常数。
N2(g)+3H2(g)的平衡常数。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中微粒的物质的量浓度关系正确的是( )
A.pH相等的①NH4Cl、②(NH4)2SO4、③NH4HSO4溶液:c(NH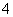 )大小顺序为①>②>③
)大小顺序为①>②>③
B.0.2 mol·L-1CH3COOH溶液和0.2 mol·L-1CH3COONa溶液等体积混合:c(CH3COOH)+c(H+)-c(OH-)=0.1 mol·L-1
C.0.1 mol·L-1 NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)=c(HCO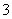 )+c(CO
)+c(CO )+c(OH-)
)+c(OH-)
D.0.1 mol·L-1的NaHA溶液,其pH=4:c(HA-)>c(H+)>c(H2A)>c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a-的电子层结构与氦相
同,b和c的次外层有8个电子,c-和d+的电子层结构相同。下列叙述错误的是
A.元素的非金属性次序为c>b>a
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a 、b、c各自最高和最低化合价的代数和分别为0、4、6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com