
X、Y、Z是元素周期表中的三种短周期元素,三者的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是( )
| X | ||
| Z | Y |
A.Z一定是活泼的金属元素
B.Y不存在最高价氧化物
C.1 mol Y的单质溶于足量水时,反应转移的电子为1 mol
D.Y的氢化物稳定性大于Z的氢化物稳定性
科目:高中化学 来源: 题型:
化合物G的合成路线如下:
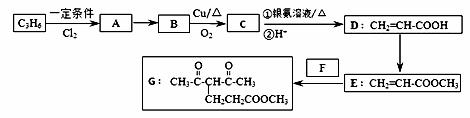
(1)D中含氧官能团的名称为 ,1 mol G发生加成反应最多消耗 mol H2 。
(2)除掉E中含有少量D的试剂和分离方法分别是 , ;
(3)下列说法正确的是 (填字母序号)。
a.A易溶于水
b.只用溴水即可确定C中含有碳碳双键
c.E经加聚、碱性条件下水解,所得高聚物可做具有高吸水性能的树脂
d.E是CH2=CHCOOCH2CH3的同系物
(4)写出A→B的化学反应方程式 ;
写出C和银氨溶液反应的离子方程式 。
(5)反应E + F→ G属于下列麦克尔加成反应类型,则F的结构简式为 。
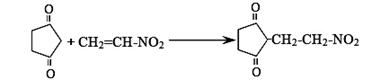

(6)比G少2个氢原子的物质具有下列性质:①遇FeCl3溶液显紫色;②苯环上的一氯取代物只有一种;③1mol物质最多可消耗2mol Na和1mol NaOH。任写一种该物质的结构简式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是元素周期表中原子序数依次增大的四种常见元素,只有W位于长周期。其相关信息如下表:
| 元素 | 相关信息 |
| X | X原子的电子层数是最外层电子数的2倍 |
| Y | Y与X同周期,该元素与氧能形成多种化合物 |
| Z | Z的基态原子的最高能级上有2个单电子,其最高价氧化物对应的水化物是一种强酸 |
| W | W是一种过渡金属元素,在潮湿的空气中其表面会生成一种绿色的化合物 |
(1)X的最高价氧化物对应的水化物的化学式为__________________________,预测该化合物________(填“难”或“易”)溶于水。
(2)Z位于元素周期表第______周期第_____族;W元素的基态原子的核外电子排布式为________________________________________________________。
(3)Y和Z的氢化物中,前者较稳定,则共价键的键长较长的物质是__________(填化学式)。
(4)Y、Z和氢元素组成的某种含氧酸正盐溶液中,Z呈现最高正价。该物质的水溶液呈酸性,其原因是___________________(填离子方程式)。
(5)W2Z能与Y的最高价氧化物对应的水化物的稀溶液反应,生成物中无难溶物,写出反应的化学方程式:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知NaHSO4在水中的电离方程式为:NaHSO4====Na++H++S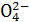 。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是( )
。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。对于该溶液,下列叙述中不正确的是( )
A.该温度下加入等体积pH=12的NaOH溶液可使反应后的溶液恰好是中性
B.水电离出来的c(H+)=1×10-10mol·L-1
C.c(H+)=c(OH-)+c(S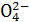 )
)
D.该温度高于25℃
查看答案和解析>>
科目:高中化学 来源: 题型:
现有常温下的六份溶液:
①0.01 mol·L-1CH3COOH溶液;
②0.01 mol·L-1HCl溶液;
③pH=12的氨水;
④pH=12的NaOH溶液;
⑤0.01 mol·L-1CH3COOH溶液与pH=12的氨水等体积混合后所得溶液;
⑥0.01 mol·L-1HCl溶液与pH=12的NaOH溶液等体积混合所得溶液。
(1)其中水的电离程度最大的是 (填序号,下同),水的电离程度相同的是 ;
(2)若将②、③混合后所得溶液pH=7,则消耗溶液的体积:② ③(填“>”“<”或“=”);
(3)将六份溶液同等稀释10倍后,溶液的pH:
① ②,③ ④,⑤ ⑥(填“>”“<”或“=”);
(4)将①、④混合,若有c(CH3COO-)>c(H+),则混合溶液可能呈 (填序号)。
A.酸性 B.碱性 C.中性
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R |
| 原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
| 主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
已知X是短周期中最活泼的金属,且与R同周期。下列叙述正确的是( )
A.离子半径大小:Y2->R3+>M2-
B.Z与M的气态氢化物的稳定性:Z>M
C.将YM2通入溶有Z的气态氢化物的BaCl2溶液中没有白色沉淀产生
D.X、Y、R的最高价氧化物的水化物两两之间能发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关等离子体的说法中,不正确的是( )
A.等离子体内部全部是带电荷的微粒
B.等离子体中正、负电荷大致相等
C.等离子体具有很好的导电性
D.等离子体用途十分广泛
查看答案和解析>>
科目:高中化学 来源: 题型:
用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式2H++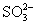 ====H2O+SO2↑的反应个数有( )
====H2O+SO2↑的反应个数有( )
A.4个 B.5个
C.8个 D.12个
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表所列数据判断,错误的是
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
A.元素X的常见化合价是+1 B.元素Y是ⅢA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第三周期,它可与冷水剧烈反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com