
| A. | 化学反应中,有放热反应也有吸热反应 | |
| B. | 煤、石油、天然气是当今世界最重要的三种化石燃料 | |
| C. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应是吸热反应 | |
| D. | 化学反应中能量变化的大小与反应物的质量多少无关 |
分析 A、化学反应的能量变化主要为热量变化,当反应物总能量大于生成物总能量为放热反应,反之为吸热反应;
B、化石燃为煤、石油、天然气;
C、Ba(OH)2•8H2O晶体与NH4Cl晶体的反应为反应物总能量小于生成物总能量;
D、化学反应的能量变化和物质的量有关,和物质的聚集状态有关.
解答 解:A、化学反应中的能量变化主要表现为热量变化,当反应物总能量大于生成物总能量为放热反应,反之为吸热反应,故A正确;
B、三大化石燃为煤、石油、天然气,故B正确;
C、Ba(OH)2•8H2O晶体与NH4Cl晶体的反应为反应物总能量小于生成物总能量,所以为吸热反应,故C正确;
D、化学反应的能量变化和物质的量有关,和物质的聚集状态有关,故D错误;
故选D.
点评 本题考查了化学反应的实质应用,吸放热反应的判断,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 生石灰用作食品抗氧化剂 | |
| B. | FeCl3溶液能被铜置换,可用于铜质印刷线路板制作 | |
| C. | 铁红常用作红色油漆和涂料 | |
| D. | 氢氧化钡可作胃酸的中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
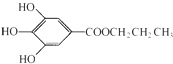 ,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.
,是白色粉末,难溶于水,微溶于棉子油等油脂,是常用的食用油抗氧化剂.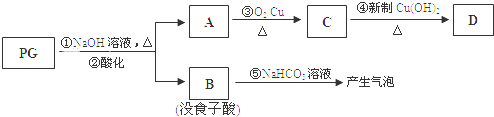
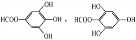
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食物储存在冰箱里 | |
| B. | 铁制品表面刷油漆 | |
| C. | 用5%H2SO4溶液代替25%H2SO4溶液与锌粒反应 | |
| D. | 用过氧化氢溶液制氧气时添加少量二氧化锰粉末 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$ 2Hg+O2 | B. | Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$ 3Fe+4CO2 | ||
| C. | Fe+CuSO4=Cu+FeSO4 | D. | 2NaCl(熔融)$\frac{\underline{\;高温\;}}{\;}$ 2Na+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
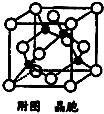
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com