
| A、3:2:2 |
| B、1:2:3 |
| C、1:3:3 |
| D、3:1:1 |


科目:高中化学 来源: 题型:
| A、氧化铝的熔点很高,因此可用做耐火材料 |
| B、氯气具有强氧化性,因此可用于漂白棉、麻、纸张 |
| C、氨很容易液化,因此可用作制冷剂 |
| D、某些金属或它们的化合物灼烧时有特殊的颜色,因此可用于制造烟花 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Na+、Cl- |
| B、SO42-、Na+、NO3-、CO32- |
| C、Na+、HCO3-、NO3-、SO42- |
| D、Fe3+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2(g)+Ca(OH)2=CaCO3↓+H2O |
| B、H2+I2?2HI |
| C、NaCl+AgNO3=AgCl↓+NaNO3 |
| D、N2+3H2?2NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向Ca(HCO3)2溶液中加入过量NaOH溶液,有白色沉淀生成:Ca2++HCO3-+OH-═CaCO3↓+H2O |
| B、磷酸一氢钠溶液水解:HPO42-+H2O?PO43-+H3O+ |
| C、将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ/mol |
| D、向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:x>y |
| B、电负性:x>y |
| C、离子半径:x<y |
| D、第一电离:x<y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、非金属元素都是主族元素,单质在反应中都只能作氧化剂 |
| B、C、N、S三者的单质直接与氧气反应都能至少生成两种氧化物 |
| C、除惰性元素外,周期表中共有16 种非金属元素 |
| D、氧化物常温下都可以与水反应生成酸,所形成的含氧酸盐(MaROb)中的R 元素必定呈现正价 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分馏、裂化、裂解是利用化学变化来炼制加工石油的三种重要方法 |
| B、蛋白质、淀粉、纤维素都能在人体内水解并提供能量 |
C、使用聚乙烯塑料制品比使用聚乳酸 (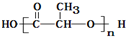 )塑料制品更环保 )塑料制品更环保 |
| D、酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对环境保护、节能减排具有重要意义 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com