
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂溶解在亚硫酰氯(SOCl2)中形成,电池总反应方程式:8Li+3SOCl2===6LiCl+Li2SO3+2S,已知将亚硫酰氯和AlCl3·6H2O混合共热蒸干,可制得无水AlCl3。则下列叙述正确的是 ( )。
A.SOCl2在制备无水AlCl3的反应中只起干燥作用
B.金属锂作电池的正极,石墨作电池的负极
C.电池工作过程中,SOCl2被还原为Li2SO3
D.电池工作过程中,消耗的锂与析出的S的质量之比为7∶8
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:
如图所示的装置中,M为活动性顺序位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,不正确的是 ( )

A.N上有气体放出
B.M为负极,N为正极
C.是化学能转化为电能的装置
D.导线中有电流通过,电流方向是由M到N
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是原子序数依次增大的五种短周期元素。A原子的电子层数与它的核外电子总数相同,A与C、B与D分别为同主族,B和C的最外层电子数之和与E的最外层电子数相同。A与E形成的化合物化学式为AE,其分子中含18个电子。请回答下列问题:
(1)A元素单质的化学式为______________________,D元素的原子结构示意图为____________________________。
(2)由A、B、C三种元素形成的化合物的电子式为_______________,这种化合物中所含的化学键类型有______________________________________。
(3)A2B的沸点高于A2D,其原因是______________________________________。
(4)B、C、E三种元素形成一种盐,此盐中三种原子个数比为1∶1∶1,在25 ℃时,将该盐溶于水,测得溶液pH>7,理由是_________________(用离子方程式表示);将该盐溶液在空气中露置一段时间后(充分光照,不考虑水分的挥发),溶液的pH近似为7,则该过程的总反应方程式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列几种物质:
①CaS ②Ar ③CaO2 ④金刚石 ⑤SiC ⑥H2O2 ⑦(NH4)2SO4 ⑧MgCl2 ⑨CH3COONa ⑩[Cu(NH3)4]SO4 (以下空格均填写序号)
(1)不含极性键的分子晶体是 ;(2)含有极性键的分子晶体是 ;
(3)只含离子键的离子晶体是 ;(4)含有极性键的原子晶体是 ;
(5)含有非极性键的离子晶体是 ;(6)含有配位键的离子晶体是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
人类生活需要能量。下列能量主要由化学变化产生的是 ( )。
A.电熨斗通电发出的热量
B.电灯通电发出的光
C.水电站利用水力产生的电能
D.液化石油气燃烧放出的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是 ( )。
A.煤气化技术的推广使用,是使煤变成清洁能源的有效途径
B.煤的干馏过程属于物理变化,通过煤干馏可得到焦炉气、煤焦油、焦炭、
粗氨水等
C.煤里主要含有碳、少量其他元素及矿物,工业上大量燃烧含硫燃料是形
成酸雨的主要原因之一
D.发生炉煤气是纯净的一氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷在不同条件下有两种热解反应:①CH4(g)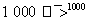 C(s)+2H2(g);②2CH4(g)
C(s)+2H2(g);②2CH4(g)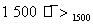 C2H2(g)+3H2(g)。现将两份标准状况下等体积的甲烷分别通入两个容积可变的密闭容器中,按①式和②式热解,待完全反应后,恢复至标准状况,则两容器中气体体积关系正确的是 ( )。
C2H2(g)+3H2(g)。现将两份标准状况下等体积的甲烷分别通入两个容积可变的密闭容器中,按①式和②式热解,待完全反应后,恢复至标准状况,则两容器中气体体积关系正确的是 ( )。
A.①和②相等 B.①小于②
C.①大于② D .无法判断
.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
某未知溶液可能含Cl-、SO32-、Na+、SO42-、Al3+,将溶液滴在红色石蕊试纸上,试纸变蓝。取少量试液,滴加硝酸酸化的氯化钡溶液,有白色沉淀生成;在上层清液中滴加硝酸银溶液,产生白色沉淀。下列判断合理的是
A.一定有Cl- B.一定有SO42-
C.一定没有Al3+ D.一定没有SO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
关于石油的说法中,不正确的是( )
A.石油主要含烃类物质,这些烃类物质随着烃分子含有的碳原子数的增加沸点升高
B.常压分馏得到的汽油是混合物,没有固定的沸点,但石油气为纯净的丙烷
C.石油分馏不是化学变化,但裂化是化学变化
D.催化重整和加氢裂化可以提高汽油等轻质油的品质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com