
【题目】某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件对化学反应速率的影响”,进行了如下实验:
实验 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | ||
1 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
2 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
3 | 1.0 | a | 3.0 | 2.0 | 5.6 |
4 | |||||
请回答:
(1)已知KMnO4酸性溶液与H2C2O4溶液反应有CO2生成,用化学方程式表示该实验的实验原理________________________________________。
(2)a=______,设计实验2、3的目的是______________________
(3)利用实验2中数据计算,用KMnO4的浓度变化表示的反应速率为v(KMnO4)=____________。
(4)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该同学绘制图1的依据是________________________________________
②该小组同学提出的假设是_________________________________________
③请你帮助该小组同学完成实验方案,并填写表中空白。
实 验 编 号 | 室温下,试管中所加试剂及其用量/mL | 再向试 管中加 入少量 固体 | 室温下 溶液颜 色褪至 无色所 需时间 /min | |||
0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 稀硫酸 | |||
4 | 3.0 | 2.0 | 3.0 | 2.0 | t | |
④若该小组同学提出的假设成立,则其依据是__________________________________
【答案】 2KMnO4 + 5H2C2O4 +3H2SO4 =2MnSO4 + K2SO4 +10CO2↑ +8H2O 4.0 探究H2C2O4 浓度对反应速率的影响 0.015 mol/(L·min) 随着反应的进行,反应物浓度逐渐减小,速率降低 生成的Mn2+起催化作用,加快反应 MnSO4
【解析】(1)酸性高锰酸钾溶液可以将草酸氧化为二氧化碳,本身被还原为Mn2+,所以反应为:2KMnO4 + 5H2C2O4 +3H2SO4 =2MnSO4 + K2SO4 +10CO2↑ +8H2O。
(2)对于实验2、3可以看出,其他反应物相同,只有草酸用量发生变化,所以这两个实验探究的是H2C2O4 浓度对反应速率的影响,因此实验中必须保证硫酸和高锰酸钾的浓度不变,所以必须保证总体积是相等的。实验2的总体积为10mL,所以实验3总体积也是10mL,计算可得a=4.0mL。
(3)实验2中高锰酸钾的初始浓度为0.2 mol/L × 3 mL÷ 10 mL = 0.06 mol/L,溶液褪色代表高锰酸钾被完全反应,所以速率为0.06 mol/L ÷ 4 min = 0.015 mol/(L·min)。
(4)①随着反应的进行,反应物浓度逐渐减小,反应速率应该逐渐降低,所以图像中n(Mn2+)随时间变化的趋势越来越平缓,最后保持不变。
②该反应速率先加快后减慢,所以可以假设是反应生成的Mn2+对反应起到了催化作用,导致反应加快,反应后期反应物的浓度减小,所以反应减慢。
③本实验的目的是验证Mn2+对反应可以起到催化作用,所以加入少量的硫酸锰固体。
④若假设成立,则反应加快,褪色用的时间应该小于4min。


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用元素符号、离子符号或化学式回答下列问题: 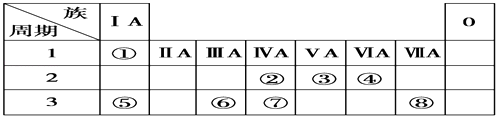
(1)④、⑥、⑧的原子半径由大到小的顺序是:(请用>、<表示) .
(2)②、③、⑧的最高价含氧酸的酸性由强到弱的顺序是: .
(3)请写出由②、④、⑦三种元素的氢化物稳定性由弱到强的顺序是: .
(4)⑤、⑥两种元素的最高价氧化物对应的水化物在溶液中相互反应的离子方程式是: .
(5)由表中两种元素的原子按1:1组成的一种常见液态化合物的稀溶液易被 催化分解,可使用的催化剂为(填序号) .
a.KMnO4b.MnO2c.Na2SO3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
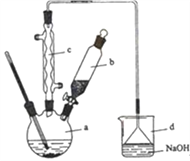
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:按下列合成步骤回答问题:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/°C | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
(1)在a中加入15 mL无水苯和少量铁屑。在b中小心加入4.0 mL液态溴。向a中滴入几滴溴,有白色烟雾产生,是因为生成了_____气体。继续滴加至液溴滴完。装置d的作用是________;制取溴苯的化学方程式____________________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是:______。
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_____;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为_______________,要进一步提纯,下列操作中必须的是_________(填入正确选项前的字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(4)取反应后烧杯中的溶液2 mL加入足量的稀硝酸酸化,再滴入AgNO3溶液,有浅黄色沉淀生成___(能或不能)证明苯与液溴反生了取代反应,为什么? _______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是( )
A.吸热反应不一定需要加热才能发生
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)△H=2×283.0 kJ/mol
C.HCl和NaOH反应的中加热△H=﹣57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ/mol
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是生命之源,下列有关“水”说法中正确的是
A. 双氧水被称为绿色氧化剂,是因为其还原产物为O2,对环境没有污染
B. 王水是浓盐酸和浓硝酸按体积比1︰3配成的混合物,可以溶解Au、Pt
C. 人们利用臭氧的强氧化性可将其用作自来水的消毒剂
D. 酸雨是指pH﹤7的雨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨反应:N2(g)+3H2(g)2NH3(g)△H=﹣92.4kJmol﹣1 , 在反应过程中,正反应速率的变化如图.下列说法正确的是( ) 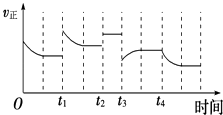
A.t1时升高了温度
B.t2时使用了催化剂
C.t3时增大了压强
D.t4时降低了温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下向蒸馏水中加入冰醋酸晶体,恢复至室温,测得溶液的pH为2.下列对该溶液的叙述中不正确的是( )
A.醋酸溶液的浓度为0.01mol/L
B.由水电离出来的H+的浓度是1.0×10﹣12 mol/L
C.冰醋酸晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(固)+nB(气)pC(气)△H<0在一定温度下B的体积分数(B%)与压强变化的关系如图所示,下列叙述中正确的是( ) 
A.m+n>P
B.n>p
C.x点表示该反应的正反应速率小于逆反应速率
D.x点比y点时的反应速率慢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com