
| A. | 加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸沉淀不消失,则原溶液中一定有SO42- | |
| B. | 通入Cl2后,溶液变为黄色,加入淀粉后溶液变蓝,则原溶液中一定有I- | |
| C. | 加入碳酸钠溶液有白色沉淀生成,再加盐酸,沉淀消失,则原溶液中一定有Ba2+ | |
| D. | 加入NaOH溶液并加热,产生使湿润的蓝色石蕊试纸变红的气体,则原溶液一定有NH4+ |
分析 A.加入Ba(NO3)2溶液生成的不溶于盐酸的白色沉淀可能为硫酸钡,原溶液中可能含有SO42-或SO32-;
B.Cl2与I-发生氧化还原反应,碘遇淀粉变蓝;
C.能够与碳酸钠生成的溶于盐酸的白色沉淀不一定为碳酸钡,可能为碳酸钙,原溶液中可能含有钙离子;
D.能使湿润蓝色石蕊试纸变红的气体为酸性气体.
解答 解:A.加入Ba(NO3)2溶液生成的不溶于盐酸的白色沉淀可能为硫酸钡,原溶液中可能含有SO32-,不一定含有SO42-,故A错误;
B.通入Cl2后,溶液变为黄色(碘水),加入淀粉后溶液变蓝(碘遇淀粉变蓝),则原溶液中一定有I-,故B正确;
C.碳酸钡和碳酸钙等沉淀都可溶于盐酸,原溶液中可能含有Ca2+,不一定含有Ba2+,故C错误;
D.产生使湿润蓝色石蕊试纸变红的气体,为酸性气体,该气体不是氨气,则原溶液中不存在氨气,故D错误;
故选B.
点评 本题考查了常见离子的检验方法,题目难度中等,试题侧重于离子检验方法的评价,注意把握常见离子的性质以及检验方法,明确检验离子的存在情况时要排除其它离子的干扰.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 电负性的大小顺序为Cl>S>P | |
| B. | 由于NO3-和SO3互为等电子体,所以可以推断NO3-的空间构型为平面三角形 | |
| C. | 根据晶格能的大小可以判断MgCl2的熔点比CaCl2高 | |
| D. | 液态HF的沸点比液态HCl的沸点高是因为氢氟键的键能比氢氯键的键能大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池工作时,锌失去电子 | |
| B. | 电池工作时,电子由正极通过外电路流向负极 | |
| C. | 电池正极的电极反应式为:2MnO2+H2O+2e-═Mn2O3+2OH- | |
| D. | 外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,
,
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 25℃时,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 常温下干燥的Cl2能用钢瓶贮运,所以Cl2在任何条件下都不与铁反应 | |
| D. | 图示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
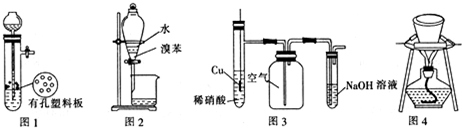
| A. | 图1装置用于Cu和浓H2SO4反应制取少量的SO2气体 | |
| B. | 图2装置用于分离水和溴苯的混合物 | |
| C. | 图3装置用于制备并收集NO气体 | |
| D. | 图4装置用于除去碳酸氢钠固体中的少量碳酸钠 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com