
【题目】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O] 俗称莫尔盐,可溶于水,在100℃~110℃时分解。在定量分析中常用作标定重铬酸钾、高锰酸钾等溶液的标准物质,还用于冶金、电镀等。
Ⅰ.化学课外活动小组研究莫尔盐晶体强热时的分解产物。
(1)甲组同学按照如图所示的装置进行研究,装置C中可观察到的现象是__________,由此可知分解产物中有____________。
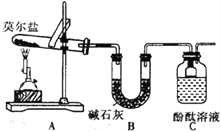
(2)乙组同学认为莫尔盐晶体分解的产物中还含有SO3(g)、SO2(g)及N2。为进行验证,选用甲组实验中的装置A和下图所示的部分装置进行实验。
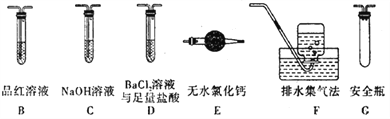
①乙组同学的实验中,装置依次连接的合理顺序为A、____________。
②含有SO3的实验现象是______________;
Ⅱ.为测硫酸亚铁铵纯度,称取m g莫尔盐样品,配成500mL溶液。甲、乙、丙三位同学设计了如下三个实验方案,请回答:
甲方案:取25.00mL硫酸亚铁铵溶液用0.1000mol·L-1的酸性KMnO4溶液分三次进行滴定。
乙方案:取25.00 mL硫酸亚铁铵溶液进行如下实验。
![]()
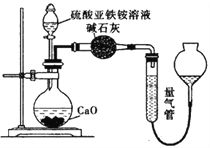
丙方案:(通过![]() 测定)实验设计图如下所示。取25.00mL硫酸亚铁铵溶液进行该实验。
测定)实验设计图如下所示。取25.00mL硫酸亚铁铵溶液进行该实验。
(1)甲方案中的离子方程式为___________,若实验操作都正确,但其测定结果总是小于乙方案,可能原因为___________。
(2)乙方案中沉淀是否洗涤干净的检验方法是________________。
(3)丙方案中量气管中最佳试剂是______________。
a.水 b.饱和NaHCO3溶液 c.CCl4
(4)若测得NH3(已折算为标准状况下)为V L,则硫酸亚铁铵纯度为_____________。
【答案】 溶液变红 NH3 G D B C F D中出现白色沉淀 MnO4- + 5Fe2+ 8H+ = Mn2+ + 5Fe3+ + 4H2O Fe2+已被空气部分氧化 取最后一次洗涤的滤液加入AgNO3溶液,若没有沉淀,说明已洗干净 c 175V/m或![]()
【解析】Ⅰ.(1)莫尔盐硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O] 受热分解,分解产生氨气和二氧化硫、三氧化硫等酸性气体,由装置图,碱石灰可以吸收酸性气体,氨气遇到酚酞溶液变红色,装置C中可观察到的现象是溶液变红,可知莫尔盐晶体分解的产物中有 NH3;(2)①要检验生成SO3(g)、SO2(g)及N2,在甲组实验中的装置A产生气体后,经过安全瓶后通过氯化钡溶液检验SO3,再通过品红溶液检验SO2,用浓氢氧化钠除去二氧化硫,用排水集气法收集氮气,所以装置依次连接的合理顺序为A、G、D、B、C、F;②由于产生的气体中有氨气,所以氯化钡溶液中加入足量的盐酸,可以吸收氨气并防止产生亚硫酸钡沉淀,排除SO2的干扰,SO3通入氯化钡溶液中可以产生硫酸钡沉淀,二氧化硫能使品红褪色,含有SO3的实验现象是:D中有白色沉淀;Ⅱ.(1)高锰酸钾溶液具有氧化性,能氧化亚铁离子为铁离子,反应离子方程式为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,亚铁离子具有还原性,易被空气中的氧气氧化成铁离子;(2)乙方案中沉淀是否洗涤干净,可以设计实验检验洗涤液中是否含有氯离子检验沉淀洗涤是否干净,具体步骤为:取最后一次洗涤的滤液加入AgNO3溶液,若没有沉淀,说明已洗干净;(3)丙方案中,量气管中液体应不能溶解氨气,氨气易溶于水和饱和碳酸钠溶液,难溶于四氯化碳,故用排四氯化碳法收集,故选c;
(4)VL氨气的物质的量为:![]() =
=![]() mol,m g硫酸亚铁铵样品中含N的物质的量为
mol,m g硫酸亚铁铵样品中含N的物质的量为![]() ×
×![]() mol=
mol=![]() mol,硫酸亚铁铵的纯度为:
mol,硫酸亚铁铵的纯度为:![]() ×100%=
×100%=![]() ×100%。
×100%。


科目:高中化学 来源: 题型:
【题目】实验室里常用的干燥剂有:①浓硫酸(98%),②无水氯化钙,③变色硅胶[硅胶的主要成分是二氧化硅,在其中掺入少量的无水氯化钴(CoCl2)作指示剂,无水氯化钴呈蓝色,吸水后变为CoCl2·6H2O呈粉红色],④五氧化二磷,⑤碱石灰(主要成分是氢氧化钠、氧化钙,制法是:把生石灰加到浓的烧碱溶液中,再加强热蒸干)。上述物质中,属于混合物的是( )
A.①②④B.②④C.①③⑤D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物数目非常庞大,是由多种原因造成的,下列说法不确切的是( )
A.碳原子间可形成单键、双键、三键
B.碳链上碳原子可以与多种原子(或原子团)形成共价键
C.碳链化合物都非常稳定
D.碳链化合物能形成各种同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国丝绸有五千年的历史和文化。古代染坊常用某种“碱剂”来精炼丝绸,该“碱剂”的主要成分是一种盐,能促进蚕丝表层的丝胶蛋白杂质水解而除去,使丝绸颜色洁白、质感柔软、色泽光亮。这种“碱剂”主要成分可能是( )
A.氢氧化钾B.次氯酸钙C.烧碱D.碳酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)具有耐高温.抗冲击.导热性好等优良性质,被广泛应用于电子工业.陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:
Al2O3+N2+3C ![]() 2AlN+3CO下列叙述正确的是( )
2AlN+3CO下列叙述正确的是( )
A.在氮化铝的合成反应中,N2是还原剂,Al2O3氧化剂
B.氮化铝是铝合金中的一种
C.上述反应中每生成2molAlN,N失去6mol电子
D.氮化铝中氮元素的化合价为﹣3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁元素在地壳中的含量丰富。关于铁及其化合物的说法错误的是( )
A. 铁合金是使用最早的合金 B. Fe2O3 常用作红色油漆的原料
C. Fe(OH)3 胶体可做净水剂 D. Fe3O4 是具有磁性的黑色晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将固体NH4Br置于密闭容器中,在某温度下,发生下列可逆反应:NH4Br(s) ![]() NH3(g)+HBr(g) 2HBr(g)
NH3(g)+HBr(g) 2HBr(g) ![]() Br2(g)+H2(g),2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用
Br2(g)+H2(g),2min后,测得c(H2)=0.5mol/L,c(HBr)=4mol/L,若上述反应速率用![]() (NH3)表示,下列反应速率正确的是
(NH3)表示,下列反应速率正确的是
A.0.5mol/(L·min) B.2.5 mol/(L·min)
C.2 mol/(L·min) D.5 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图装置中,b电极用金属M制成,a、c、d为石墨电极,接通电源,金属M沉积于b极,同时a、d电极上产生气泡。试回答:

(1)c极的电极反应式为________ 。
(2)电解开始时,在B烧杯的中央,滴几滴淀粉溶液,电解进行一段时间后,你能观察到的
现象是:___________,电解进行一段时间后,罩在c极上的试管中也收集到了气体,此时c极上的电极反应式为_____________。
(3)当d极上收集到44.8mL气体(标准状况)时停止电解,a极上放出了____moL气体,
此时若b电极上沉积金属M的质量为0.432g,则此金属的摩尔质量为___________。
此时A池中溶液氢离子的浓度为_________mol/L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com