
¶ŌÓŚ»Æѧ·“Ó¦3W£Øg£©£«2X£Øg£©==4Y£Øg£©£«3Z£Øg£©£¬ĻĀĮŠ·“Ó¦ĖŁĀŹ¹ŲĻµÖŠ£¬ÕżČ·µÄŹĒ£Ø £©
A£®v£ØW£©£½3v£ØZ£© B£®2v£ØX£©£½3v£ØZ£© C£®2v£ØX£©£½v£ØY£© D£®3v£ØW£©£½2v£ØX£©
 Č«³Ģ½š¾ķĻµĮŠ“š°ø
Č«³Ģ½š¾ķĻµĮŠ“š°ø æģĄÖ5¼Ó2½š¾ķĻµĮŠ“š°ø
æģĄÖ5¼Ó2½š¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ČŻĘ÷ | ¼× | ŅŅ | ±ū |
| ·“Ó¦ĪļĶ¶ČėĮæ | 1mol N2”¢3mol H2 | 2mol NH3 | 4mol NH3 |
| Ę½ŗāŹ±NH3µÄÅØ¶Č£Ømol•L-1£© | cl | c2 | c3 |
| ·“Ó¦µÄÄÜĮæ±ä»Æ | ·Å³öa kJ | ĪüŹÕbkJ | ĪüŹÕc kj |
| ĢåĻµŃ¹Ēæ£Øpa£© | p1 | p2 | p3 |
| ·“Ó¦Īļ×Ŗ»ÆĀŹ | a1 | a2 | a3 |

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗžÄĻŹ”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
1.56 gĻŌ£«1¼ŪµÄij½šŹōÓė×ćĮæŃĪĖįĶźČ«·“Ó¦£¬Éś³É0.04 gĒāĘų£¬ŌņøĆ½šŹōµÄĦ¶ūÖŹĮæĪŖ______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗžÄĻŹ”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲŅĒĘ÷µÄŹ¹ÓĆÕżČ·µÄŹĒ£Ø £©
A. ŹÖ³ÖŹŌ¹ÜøųŹŌ¹ÜÄŚµÄĪļÖŹ¼ÓČČ
B. ÓĆČ¼×ÅµÄ¾Ę¾«µĘČ„µćČ¼ĮķŅ»Õµ¾Ę¾«µĘ
C. ÓĆĢģĘ½³ĘĮæŅ©Ę·Ź±ÓĆŹÖÖ±½ÓÄĆķĄĀė
D. ÓƵĪ¹ÜµĪ¼ÓŅŗĢåŹ±µĪ¹ÜÓ¦“¹Ö±Šü“¹ŌŚČŻĘ÷ÉĻ·½ĒŅ²»ÄÜ“„¼°ČŻĘ÷ÄŚ±Ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓÄĻŹ”ŠĀĻēŹŠø߶žÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
£ØĆææÕ3·Ö£¬¹²6·Ö£©øł¾ŻĻĀĮŠŠšŹöŠ“³öĻąÓ¦µÄČČ»Æѧ·½³ĢŹ½£ŗ
£Ø1£©ŅŃÖŖ16 g¹ĢĢåĮņĶźČ«Č¼ÉÕŹ±·Å³ö148.4 kJµÄČČĮ棬Š“³ö±ķŹ¾ĮņµÄČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½£ŗ______________”£
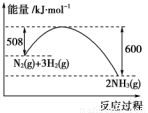
£Ø2£©ČēĶ¼ŹĒ298 K”¢101 kPaŹ±£¬N2ÓėH2·“Ó¦¹ż³ĢÖŠÄÜĮæ±ä»ÆµÄĒśĻßĶ¼”£øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŗÓÄĻŹ”ŠĀĻēŹŠø߶žÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ·Ö±šŹĒĄūÓĆ²»Ķ¬ÄÜŌ“·¢µēµÄŹµĄżĶ¼ŠĪ£¬ĘäÖŠ²»ŹōÓŚŠĀÄÜŌ“æŖ·¢ĄūÓƵďĒ£Ø £©

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğÖŲĒģŹŠø߶žÉĻ°ėĘŚæ¼ŹŌ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŗĻ³É°±ŹĒČĖĄąæĘѧ¼¼ŹõÉĻµÄŅ»ĻīÖŲ“óĶ»ĘĘ£¬Ęä·“Ó¦ŌĄķĪŖN2£Øg£©£«3H2£Øg£© 2NH3£Øg£© ¦¤H£½£92.4 kJ”¤mol£1”£Ņ»ÖÖ¹¤ŅµŗĻ³É°±µÄ¼ņŹ½Į÷³ĢĶ¼ČēĻĀ£ŗ
2NH3£Øg£© ¦¤H£½£92.4 kJ”¤mol£1”£Ņ»ÖÖ¹¤ŅµŗĻ³É°±µÄ¼ņŹ½Į÷³ĢĶ¼ČēĻĀ£ŗ
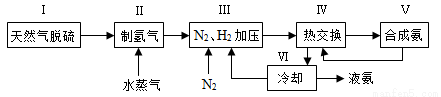
£Ø1£©ĢģČ»ĘųÖŠµÄH2SŌÓÖŹ³£ÓĆ°±Ė®ĪüŹÕ£¬²śĪļĪŖNH4HS”£Ņ»¶ØĢõ¼žĻĀĻņNH4HSČÜŅŗÖŠĶØČėæÕĘų£¬µĆµ½µ„ÖŹĮņ²¢Ź¹ĪüŹÕŅŗŌŁÉś£¬Š“³öŌŁÉś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ____________________”£
£Ø2£©²½Öč¢ņÖŠÖĘĒāĘųµÄŌĄķČēĻĀ£ŗ
¢ŁCH4£Øg£©£«H2O£Øg£© CO£Øg£©£«3H2£Øg£©¦¤H£½£«206.4kJ”¤mol£1
CO£Øg£©£«3H2£Øg£©¦¤H£½£«206.4kJ”¤mol£1
¢ŚCO£Øg£©£«H2O£Øg£© CO2£Øg£©£«H2£Øg£©¦¤H£½£41.2kJ”¤mol£1
CO2£Øg£©£«H2£Øg£©¦¤H£½£41.2kJ”¤mol£1
¶ŌÓŚ·“Ó¦¢Ł£¬Ņ»¶ØæÉŅŌĢįøßĘ½ŗāĢåĻµÖŠH2µÄ°Ł·Öŗ¬Į棬ÓÖÄܼÓæģ·“Ó¦ĖŁĀŹµÄ“ėŹ©ŹĒ __”£
ĄūÓĆ·“Ó¦¢Ś£¬½«CO½ųŅ»²½×Ŗ»Æ£¬æÉĢįøßH2µÄ²śĮ攣Čō1 mol COŗĶH2µÄ»ģŗĻĘųĢå£ØCOµÄĢå»ż·ÖŹżĪŖ20%£©ÓėH2O·“Ó¦£¬µĆµ½1.18 mol CO”¢CO2ŗĶH2µÄ»ģŗĻĘųĢ壬ŌņCOµÄ×Ŗ»ÆĀŹĪŖ____________”£
£Ø3£©Ķ¼£Øa£©±ķŹ¾500 ”ę”¢60.0 MPaĢõ¼žĻĀ£¬ŌĮĻĘųĶ¶ĮĻ±ČÓėĘ½ŗāŹ±NH3Ģå»ż·ÖŹżµÄ¹ŲĻµ”£øł¾ŻĶ¼ÖŠaµćŹż¾Ż¼ĘĖćN2µÄĘ½ŗāĢå»ż·ÖŹż£ŗ____________”£
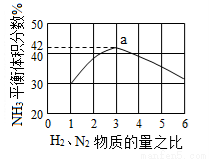
£Ø4£©ÉĻŹöĮ÷³ĢĶ¼ÖŠ£¬Ź¹ŗĻ³É°±·Å³öµÄÄÜĮæµĆµ½³ä·ÖĄūÓƵÄÖ÷ŅŖ²½ÖčŹĒ£ØĢīŠņŗÅ£©_____________”£¼ņŹö±¾Į÷³ĢÖŠĢįøßŗĻ³É°±ŌĮĻ×Ü×Ŗ»ÆĀŹµÄ·½·Ø£ŗ_____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğÖŲĒģŹŠø߶žÉĻ°ėĘŚæ¼ŹŌ»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¶ŌÓŚŌŚĆܱÕČŻĘ÷ÖŠ”¢Ņ»¶ØĢõ¼žĻĀ½ųŠŠµÄæÉÄę·“Ó¦N2£Øg£©£«3H2£Øg£© 2NH3£Øg£©£¬ÄÜĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ
2NH3£Øg£©£¬ÄÜĖµĆ÷·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ
A£®ø÷ĪļÖŹĢå»ż·ÖŹżĻąµČ B£®c£ØNH3£©±£³Ö²»±ä
C£®ø÷ĪļÖŹÅضČĻąµČ D£®c£ØNH3£©”Ćc£ØN2£©”Ćc£ØH2£©=2”Ć1”Ć3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
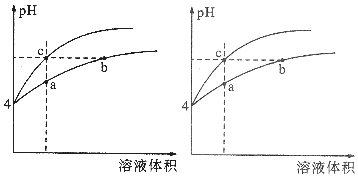 ijĪĀ¶ČĻĀ£¬Ģå»żŗĶpH¶¼ĻąĶ¬µÄŃĪĖįŗĶĀČ»Æļ§ČÜŅŗ¼ÓĖ®Ļ”ŹĶŹ±µÄpH±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
ijĪĀ¶ČĻĀ£¬Ģå»żŗĶpH¶¼ĻąĶ¬µÄŃĪĖįŗĶĀČ»Æļ§ČÜŅŗ¼ÓĖ®Ļ”ŹĶŹ±µÄpH±ä»ÆĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | a”¢cĮ½µćČÜŅŗµÄµ¼µēÄÜĮ¦ĻąĶ¬ | |
| B£® | bµćČÜŅŗÖŠc£ØH+£©+c£ØNH3•H2O£©=c£ØOH-£© | |
| C£® | ÓƵČÅØ¶ČµÄNaOHČÜŅŗŗĶµČĢå»żb”¢c“¦ČÜŅŗ·“Ó¦£¬ĻūŗÄNaOHČÜŅŗµÄĢå»żVb£¾Vc | |
| D£® | a”¢b”¢cČżµćČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Ča£¾b£¾c |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com