

分析 氯气通过A装置与空气形成1:3的混合气体通入B装置,在搅拌棒的作用下与含水8%的碳酸钠充分反应制备Cl2O,并用水吸收Cl2O制备次氯酸钠溶液,同时用碱石灰吸收含有Cl2O的尾气,防止污染环境,
(1)①控制氯气与空气体积比的方法可以通过观察A中产生气泡的比例来调节气体的流速;
②增加气体与溶液的接触面积、搅拌等措施都可以加快反应速率;
(2)①装置B中,氯气本身既作为氧化剂又作还原剂,本身被氧化到+1价的Cl2O,被还原到-1价的氯化钠;
②由于该反应为放热反应,温度升高Cl2O会分解,故进入C中的Cl2O会大量减少;
(3)装置C是用水吸收Cl2O制备次氯酸溶液,但生成的HClO见光易分解,反应装置须选择避光;
(4)需要20.00mL的次氯酸溶液,根据精确度应选用酸、碱式滴管,再根据HClO溶液既有酸性,又有强氧化性确定滴定管的类型;实验原理是结合所提供的试剂H2O2是还原HClO生成Cl-,再滴加过量提供的硝酸银溶液,根据生成的AgCl沉淀质量计算原溶液HClO的浓度.
解答 解:(1)①氯气和空气按照体积比约1:3混合通入潮湿碳酸钠中,控制氯气与空气体积比的方法可以通过观察A中产生气泡的比例来调节气体的流速,
故答案为:通过观察A中产生气泡的速率调节流速;
②为了氯气和原溶液充分接触完全反应,可以通过增加气体与溶液的接触面积、并用搅拌棒搅拌等方法,
故答案为:搅拌、使用多孔球泡;
(2)①装置B中,氯气本身既作为氧化剂又作还原剂,本身被氧化到+1价的Cl2O,被还原到-1价的氯化钠,故化学方程式为2Cl2+Na2CO3═Cl2O+2NaCl+CO2,
故答案为:2Cl2+Na2CO3═Cl2O+2NaCl+CO2;
(4)由于该反应为放热反应,温度升高Cl2O会分解,故进入C中的Cl2O会大量减少,
故答案为:该反应放热,温度升高Cl2O会分解;
(3)装置C中使用棕色平底烧瓶,目的是可以避光,防止反应生成的HClO见光分解,
故答案为:HClO见光易分解;
(4)选择使用酸式滴定管量取20.00mL的次氯酸溶液,具体实验操作是,向20.00mL的次氯酸溶液里加入足量的H2O2溶液,再加入足量的硝酸银溶液,过滤、洗涤,在真空干燥箱中干燥沉淀,用电子天平称量沉淀的质量,
故答案为:酸式滴定管; 加入足量的H2O2溶液,再加入足量的硝酸银溶液,过滤,洗涤,在真空干燥箱中干燥,用电子天平称量沉淀质量.
点评 本题考查了物质的制备和性质实验,涉及电解原理的应用、实验的基本操作及滴定原理应用与计算,根据题目给定的基本信息解题,理清整个制备的流程及操作方法是解题的关键,要求具备扎实的基础知识和分析问题的能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ①②③ | D. | ①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向稀HNO3中滴加Na2SO3溶液:2H++SO32-═SO2↑+H2O | |
| B. | 向Al2(SO4)3溶液中加入过量的NaOH溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | 向0.1mol/L pH=1的KHA溶液中加入KOH溶液:H++OH-═H2O | |
| D. | 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-═2Mn2++10CO2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 反应条件 | 时间 | NO/mol | Cl2/mol | NOCl/mol |
| 实验① | T、恒容 | 初始 | 0.2 | 0.1 | 0 |
| 10 min | 0.05 | 0.025 | |||
| 12 min | 0.15 | ||||
| 实验② | T、恒压 | 初始 | 0.2 | 0.1 | 0 |
| A. | 实验①中,0~10min内,v(NOCl)=7.5×10-3 mol•L-1•min-1 | |
| B. | 平衡时若升高温度,达到新平衡时K=400,则该反应△H>0 | |
| C. | 平衡时实验②比实验①的Cl2转化率大 | |
| D. | 若实验①起始只充入0.4molNOCl,则平衡时NOCl浓度大于0.15mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
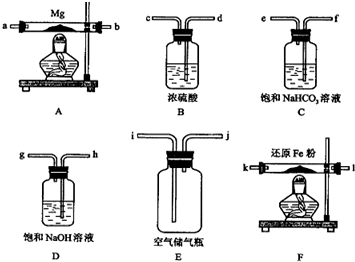
| 装置 | 目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
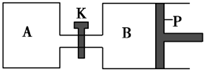 如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ•mol-1(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向A、B容器中分别充入2mol A2和1mol B2,两容器分别在500℃时达平衡,A中C的浓度为w1 mol•L-1,放出热量b kJ,B中C的浓度为w2 mol•L-1,放出热量c kJ.下列说法错误的是( )
如图所示的装置中发生反应2A2(g)+B2(g)?2C(g)△H=-a kJ•mol-1(a>0),已知P是可自由滑动的活塞.在相同温度时关闭K,向A、B容器中分别充入2mol A2和1mol B2,两容器分别在500℃时达平衡,A中C的浓度为w1 mol•L-1,放出热量b kJ,B中C的浓度为w2 mol•L-1,放出热量c kJ.下列说法错误的是( )| A. | 此反应的平衡常数表达式为K=$\frac{{c}^{2}(C)}{{c}^{2}({A}_{2})•c({B}_{2})}$ | |
| B. | C的浓度大小比较为:w2<w1 | |
| C. | a、b、c由大到小的关系为a>c>b | |
| D. | 若打开K,一段时间后重新达平衡,容器B的体积将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com