
| A. | 溶液 | B. | 胶体 | C. | 悬浊液 | D. | 乳浊液 |
 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
| A. | 萃取时,要求萃取剂的密度比水的密度大 | |
| B. | 蒸馏时,温度计水银球与蒸馏烧瓶支管口相平 | |
| C. | 过滤时,要将待过滤混合物转移到漏斗中 | |
| D. | 分液时,分液漏斗的下口必须紧贴在烧杯壁上 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
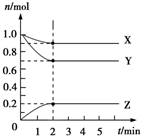 Ⅰ.控制变量法是化学实验的一种常用方法.下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
Ⅰ.控制变量法是化学实验的一种常用方法.下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用铁片和稀硫酸反应制氢气时,滴入几滴硫酸铜溶液可以加快反应速率 | |
| B. | 汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率变慢 | |
| C. | SO2的催化氧化反应是一个放热的反应,所以升高温度,反应速率变慢 | |
| D. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )
)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
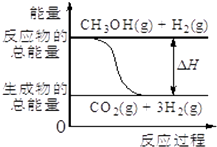 已知CH3OH(g)+H2O(g)=CO2(g)+3H2(g),该反应中的能量变化如图所示下列说法不正确的是( )
已知CH3OH(g)+H2O(g)=CO2(g)+3H2(g),该反应中的能量变化如图所示下列说法不正确的是( )| A. | 该反应拆开反应物所有键所吸收的总能量小于形成生成物所放出的总能量 | |
| B. | 该反应是放热反应 | |
| C. | 该反应不能设计成原电池 | |
| D. | 该反应所有分子中各原子都以共价键相结合? |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃料电池工作时O2在正极上发生氧化反应 | |
| B. | 燃料电池在工作时需要点燃甲烷 | |
| C. | 燃料电池工作时燃料在负极上发生氧化反应 | |
| D. | 燃料电池工作时负极的电极反应式为:2H2O+O2+4e-=4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①② | C. | ②③ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{O}_{3}^{-})}$=$\frac{1}{5}$ | |
| B. | 参加反应的被还原的氯气为$\frac{1}{4}$amol | |
| C. | 改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$amol≤ne≤$\frac{5}{6}$amol | |
| D. | 改变温度,产物中KClO3的最大理论产量为$\frac{5}{6}$amol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com