
| A | ����ʹ������Ȼ�̼��Һ��ɫ���ڱ���ģ��Ϊ ��������ˮ��һ�������·�Ӧ����C ��������ˮ��һ�������·�Ӧ����C |
| B | ����C��H����Ԫ����ɣ������ģ��Ϊ |
| C | ����C��H��O����Ԫ����ɣ�������Na��Ӧ����������NaOH��Һ��Ӧ��������E��Ӧ������Է�������Ϊ100���� |
| D | ����Է���������C��2��������C�������ɣ� |
| E | ����C��H��O����Ԫ����ɣ������ģ��Ϊ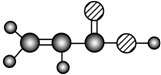 |
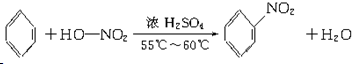 ��
������ Aʹ������Ȼ�̼��Һ��ɫ�����в����ͼ�����������ģ�Ϳ�֪��AΪCH2=CH2��A����ˮ��һ�������·�Ӧ����C��C��C��H��O����Ԫ����ɣ�����Na��Ӧ����CΪCH3CH2OH��B��C��H����Ԫ����ɣ�������ģ��֪��B��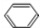 ��D����Է���������C��2��������C�������õ�������D��CH3CHO��E��C��H��O����Ԫ����ɣ���E�Ľṹ��ʽ��֪EΪCH2=CHCOOH���ݴ˽��
��D����Է���������C��2��������C�������õ�������D��CH3CHO��E��C��H��O����Ԫ����ɣ���E�Ľṹ��ʽ��֪EΪCH2=CHCOOH���ݴ˽��
��� �⣺Aʹ������Ȼ�̼��Һ��ɫ�����в����ͼ�����������ģ�Ϳ�֪��AΪCH2=CH2��A����ˮ��һ�������·�Ӧ����C��C��C��H��O����Ԫ����ɣ�����Na��Ӧ����CΪCH3CH2OH��B��C��H����Ԫ����ɣ�������ģ��֪��B�� ��D����Է���������C��2��������C�������õ�������D��CH3CHO��E��C��H��O����Ԫ����ɣ���E�Ľṹ��ʽ��֪EΪCH2=CHCOOH��
��D����Է���������C��2��������C�������õ�������D��CH3CHO��E��C��H��O����Ԫ����ɣ���E�Ľṹ��ʽ��֪EΪCH2=CHCOOH��
��1��AΪ��ϩ�����巢���ӳɷ�Ӧ����1��2-�������飬�ʴ�Ϊ��1��2-�������飻
��2��A�����������ӳɷ�Ӧ����������FΪ���飬��������̼ԭ����ĿΪ4ʱ��ʼ����ͬ���칹�壬�ʴ�Ϊ��4��
��3��B�DZ���������ɫ��������ζ�ġ�������ˮ���ܶ�С��ˮ���ж�Һ�壬������KMnO4��Һ����ˮ������Ӧ���ڴ��������¿������������ӳɷ�Ӧ��
��Ũ������������Ũ�����ڼ����������·���ȡ����Ӧ��������������Ӧ�ķ���ʽΪ ��
��
�ʴ�Ϊ���ڢۣ� ��
��
��4�����л����̼ԭ�������л���C��̼ԭ������1��ӦΪ�״��������ϵĵ缫��ӦʽΪ CH3OH-6e-+8OH-=CO32-+6H2O�������·ͨ��1.2mol e-ʱ������0.2mol�״�������Ϊ0.2mol��32g/mol=6.4g��
�ʴ�Ϊ��CH3OH-6e-+8OH-=CO32-+6H2O��6.4��
���� �����⿼�����л�����ƶϣ��ѶȲ�����ȷ���ʾ��еĹ�����ȷ������е����ʣ�ע����л��ṹģ�͵����⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������Һ�����ڼ��CO���壬ʵ�����о���װ����ͼ��
������Һ�����ڼ��CO���壬ʵ�����о���װ����ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
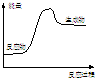
| A�� | �������ռӦ | B�� | ��˿��������Ӧ | C�� | �����ƺ�ˮ��Ӧ | D�� | ̼��ƷֽⷴӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
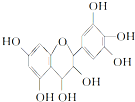
| A�� | �����ʼȿɿ������࣬Ҳ�ɿ������� | |
| B�� | 1 mol�����ʿ���4 mol Br2��Ӧ | |
| C�� | 1 mol�����ʿ���7 mol NaOH��Ӧ | |
| D�� | 1 mol�����ʿ���7 mol Na��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ���ʱ�Ϊ��ֵ | |
| B�� | ���º����£�����ѹǿ��H2Ũ��һ����С | |
| C�� | �����¶ȣ��淴Ӧ���ʼ�С | |
| D�� | �÷�Ӧ��ѧ����ʽΪCO2��g��+H2��g�� $?_{����}^{����}$ CO��g��+H2O��g�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | +319.68kJ•mol-1 | B�� | +259.7kJ•mol-1 | C�� | -319.68kJ•mol-1 | D�� | -259.7kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 CH3COOC2H5+H2O��
CH3COOC2H5+H2O�� ��Ũ���������£���Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��C6H6+HNO3$��_{50��-60��}^{Ũ����}$C6H5NO2+H2O��
��Ũ���������£���Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��C6H6+HNO3$��_{50��-60��}^{Ũ����}$C6H5NO2+H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| �� | �� | �� | �� | |||||
| �� | �� | �� | �� | �� | �� |

 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����˻�ѧ��Ӧ���ʱ� | |
| B�� | ������ͬ�ȳ̶ȵؼӿ����淴Ӧ���� | |
| C�� | �����˷�Ӧ����Ļ�� | |
| D�� | ø���и߶ȵĴ����Ժ�רһ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com