
【题目】向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图(忽略CO2的溶解和HCl的挥发)。则下列分析都正确的组合是
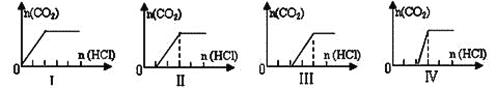
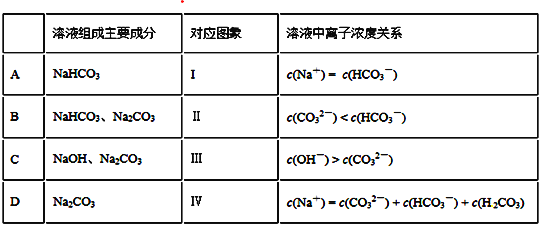
A. A B. B C. C D. D
【答案】B
【解析】向一定量NaOH溶液的烧杯中通入不同量的CO2气体,当二氧化碳少量时,产物是NaOH和Na2CO3的混合物,当NaOH和CO2恰好完全反应时,产物只有Na2CO3的,当二氧化碳过量时,产物可能只有NaHCO3,也可能是Na2CO3和NaHCO3的混合物。A、图中刚开始加入HCl就产生了二氧化碳,因此溶质只能是NaHCO3,由于碳酸氢根水解,故c(Na+)>c(HCO3-),选项A错误;B、从图中看出刚滴下去盐酸一个单位后产生了二氧化碳,说明此时碳酸根的量是一个单位(盐多酸少,碳酸钠和盐酸按1:1反应生成碳酸氢钠),后来盐酸加了两个单位才把所有二氧化碳反应放出,说明溶液中总的碳酸氢根量为两个单位,但有一个单位的碳酸氢根是之前碳酸根得来的,所以原溶液中碳酸根的量和碳酸氢根的量相等,由于碳酸钠水解程度大于碳酸氢钠,故c(CO32-)<c(HCO3-),选项B正确;C、从图中看出,滴入了两个单位的盐酸后才开始产生气泡,说明产物是NaOH和Na2CO3的混合物,一个单位的盐酸和NaOH反应,第二个单位的盐酸和Na2CO3反应生成NaHCO3,后由图中可看出,NaHCO3又消耗了2个单位的盐酸,不可能存在此种情况,选项C错误;D、从图中看出,滴入了两个单位的盐酸后才开始产生气泡,且产生二氧化碳所消耗的盐酸是一个单位,不可能只有Na2CO3,选项D错误。答案选B。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
【题目】将FeCl3、CuCl2混合溶液加入一定质量的铁粉中充分反应,所加混合溶液的体积与反应后剩余固体质量如图所示。已知原混合溶液中Fe3+浓度为0.200 mol/L,经检测M点时溶液中无Cu2+;

求:
(1)c(CuCl2 )=______mol·L-1。
(2)铁粉的质量_______g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将标准状况下的11.2 L甲烷和22.4 L氧气混合点燃,恢复到原状况后,气体的体积为( )
A.11.2 L B.22.4 L C.33.6 L D.44.8 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于反应过程中能量变化的说法正确的是( )
A.在一定条件下,某可逆反应的△H=+100kJmol﹣1 , 则该反应正反应活化能比逆反应活化能大100kJmol﹣1
B.图中A、B曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H>0未使用和使用催化剂时,反应过程中的能量变化
C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
D.己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2 . 则△H1>△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NO2装入带有活塞的密闭容器中,当反应2NO2(g)![]() N2O4(g)达到平衡后,改变下列一个条件,下列叙述正确的是
N2O4(g)达到平衡后,改变下列一个条件,下列叙述正确的是
A. 升高温度,气体颜色加深,则此反应为吸热反应
B. 慢慢压缩气体体积,平衡向正反应方向移动,混合气体的颜色变浅
C. 慢慢压缩气体体积,若体积减小一半,压强增大,但小于原来的两倍
D. 恒温恒容时,充入稀有气体,压强增大,平衡向正反应方向移动,混合气体的颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸性锌锰干电池和碱性锌锰干电池的构造简图如下所示,比较二者的异同,回答下列问题 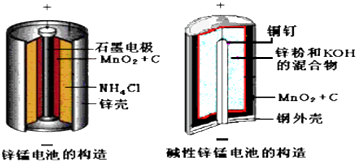
(1)酸性锌锰干电池的负极反应为 .
(2)碱性锌锰干电池在放电过程产生MnOOH,写出正极反应式 .
(3)维持电流强度为0.6A,电池工作10分钟,理论消耗Zng.(结果保留到小数点后两位,F=96500C/mol)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com