
【题目】下列实验装置(夹持和尾气处理装置已省略)进行的相应实验,能达到实验目的的是( )
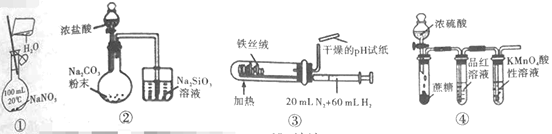
A.利用①装置,配制一定物质的量浓度的NaNO3溶液
B.利用②装置,验证元素的非金属性:Cl>C>Si
C.利用③装置,合成氨并检验氨的生成
D.利用④装置,验证浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F、G都是元素周期表中前四周期的元素,它们的原子序数依次增大。A是宇宙中含量最丰富的元素,B、D原子的L层有2个未成对电子。E3+离子M层3d轨道电子为半满状态,F比E原子序数大1且位于同一族,G的最外层只有1个电子。请根据以上情况,回答下列问题:(答题时,用所对应的元素符号表示)
(1)写出E的电子排布式____________,E位于周期表____区。
(2)B、C、D的第一电离能由小到大的顺序为___________。
(3)A、B、D三种元素可以形成组成为A2BD、A4BD、A2BD2的分子,其中B原子采取sp3 杂化的是_________(填结构简式)
(4)![]() 的空间构型为___________,键角为_______。
的空间构型为___________,键角为_______。
(5)F可形成分子式均为F(NH3)5BrSO4的两种配合物,其中一种化学式为[F(NH3)5Br]SO4往其溶液中加BaCl2溶液时,现象是_______;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时产生淡黄色沉淀,则第二种配合物的化学式为_______
(6)B元素在自然界有多种同素异形体,硬度最大晶体中每个晶胞中平均含有___个B原子。若晶胞的棱长为acm,则它的密度为____g/cm3(NA表示阿伏加德罗常数)
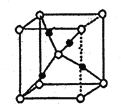
(7)G的一种氧化物M的晶胞结构如图所示(小圆圈代表氧原子),则M的化学式为________,该晶体中氧原子的配位数为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面列出了几组物质,请将物质的合适序号填写在空格上。同位素__;同一个物质__;同分异构体__;同素异形体__。
①金刚石与石墨;②D与T;③12C和13C;④O2与O3;⑤CH4和CH3-CH2-CH3;⑥CH2=CHCH3和CH2=CH2;⑦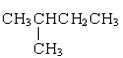 和CH3-CH2-CH2-CH2-CH3;⑧
和CH3-CH2-CH2-CH2-CH3;⑧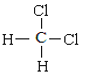 和
和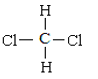
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法错误的是( )
A.1L0.2mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.2NA
B.H2O2+Cl2=2HCl+O2反应中,每生成32gO2,转移2NA个电子
C.3.6gCO和N2的混合气体含质子数为1.8NA
D.常温常压下,30g乙烷气体中所含共价键的数目为7NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用微生物燃料电池进行废水处理,可实现碳氮联合转化。某微生物燃料电池的工作原理如图所示,其中M、N为厌氧微生物电极。下列有关叙述错误的是
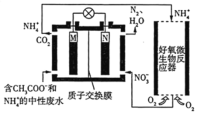
A.负极反应式为![]()
B.电池工作时,![]() 由M极区移向N极区
由M极区移向N极区
C.相同条件下,M极区生成的![]() 与N极区生成的
与N极区生成的![]() 的体积之比为
的体积之比为![]()
D.好氧微生物反应器中发生的反应的离子方程式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环氧乙烷(![]() )、环氧丙烷(
)、环氧丙烷(![]() )都是重要的化工原料且用途广泛。回答下列问题:
)都是重要的化工原料且用途广泛。回答下列问题:
(1)已知:
①![]()
![]()
②2![]()
![]()
![]()
③![]()
![]()
![]()
![]() _____
_____![]()
(2)某温度下,物质的量均为1mol的CH2=CH2和O2在0.5L的刚性容器内发生反应③,5min后反应达到平衡,气体总压减少了20%。
①平衡时CH2=CH2(g)的转化率为____,达到平衡后,欲增加CH2=CH2(g)的平衡转化率,可采取的措施是____(填一条措施即可)。
②0~5min内,环氧乙烷的生成速率为____。
③该反应的平衡常数K_____(精确到0.01)。
④当进料气CH2=CH2和O2的物质的量不变时,T1℃时达到反应平衡,请在图1中画出温度由T1℃变化到T2℃的过程中乙烯的转化率与温度的关系____。
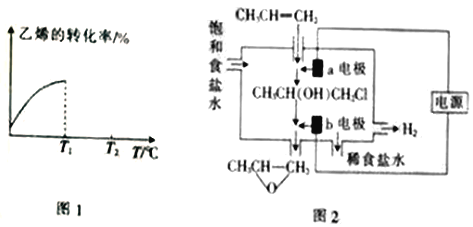
(3)将丙烯与饱和食盐水的电解产物反应,转化为氯丙醇[CH3CH(OH)CH2Cl][已知:CH3CH=CH2+H2O+Cl2→CH3CH(OH)CH2Cl+HCl],氯丙醇进一步反应生成环氧丙烷,其电解简易装置如图2所示。
①a电极上的电极反应式为______。
②b电极区域生成环氧丙烷的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(NH4ClO4)可用作火箭推进剂等。制备NH4ClO4的工艺流程如下:

(1)电解NaClO3溶液时,ClO3-在____极发生反应,其电极反应式为____。
(2)“除杂”有两种方案。
①方案1:加入盐酸和H2O2溶液,NaClO3转化为ClO2,化学方程式为______。
方案2:加入氨水和FeCl24H2O,NaClO3转化为Cl-,离子方程式为____,如果FeCl24H2O过量会出现黑色磁性沉淀,该沉淀可能是______。(填化学式)
②比较氧化性:ClO3-_____ClO4-(填“>”或“<”)。
③两种方案相比,方案1的优点是____。(答一条即可)
(3)“反应”时用NaClO4和NH4Cl在90℃制备NH4ClO4。如果用浓盐酸和液氨代替NH4Cl,则无需加热,原因是____。
(4)该流程中可循环利用的物质是_________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)以下物质中能导电且属于电解质的是__________,属于非电解质的是___________
①漂白粉 ②铜 ③氧气 ④BaSO4固体 ⑤稀硫酸 ⑥蔗糖 ⑦CO2⑧熔化的KNO3,
写出电离方程式:硫酸铝__________________________________________
(二)某化学实验小组需用480mL 0.2mol/L的硫酸铜溶液,请回答下列问题:
(1)如果用胆矾(CuSO45H2O)来配制,至少需用胆矾的质量为_____g。
(2)在该实验中要用到容量瓶,使用容量瓶前应_______________
(3)下面是配制硫酸铜溶液过程中的5个操作步骤:
①向盛有胆矾的烧杯中加入200ml蒸馏水使其溶解;
②继续往容量瓶中加蒸馏水,至液面距刻度线1-2cm处;
③将烧杯中的溶液沿玻璃棒注入容量瓶中;
④在烧杯中加入少量的蒸馏水,洗涤烧杯内壁和玻璃棒2-3次后移入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀;
⑤改用胶头滴管加水至刻度线,盖好瓶塞,反复上下颠倒,摇匀。
正确的操作顺序为__________________(填序号)
(4)上述操作⑤中,如果不小心加水超过刻度线,处理方法是_______________
(5)下列操作会导致所配硫酸铜溶液物质的量浓度偏低的是_______(填序号)
①在烧杯中搅拌溶液时,有少量液体溅出
②定容摇匀后,发现溶液液面低于刻度线,又滴加蒸馏水至刻度线
③容量瓶洗净后残留少量蒸馏水
④所使用的容量瓶刚用某种浓度的硫酸铜溶液润洗过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+2B(g)=C(g)的反应过程中能量变化如下图所示。下列相关说法正确的是

A.该反应是吸热反应
B.催化剂改变了该反应的焓变
C.曲线b表示使用催化剂后的能量变化
D.该反应的焓变![]() H= -510 kJ·mol-1
H= -510 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com