
| A. | 往0.3mol/L的NH3•H2O溶液中加入少量NaOH固体,NH3•H2O的电离平衡向逆反应方向移动,同时溶液中c(OH-)•c(NH4+)/c(NH3•H2O)将减小 | |
| B. | PH=9的NaOH溶液和NH3•H2O溶液中,由水电离出的c(H+)前者小于后者 | |
| C. | 浓度均为0.1mol/L的CH3COOH与CH3COONa溶液等体积混合后,PH=5,则混合溶液中:c(CH3COO-)-c(CH3COOH)=2×(10-5-10-9)mol/L | |
| D. | 相同条件下,将足量的氢氧化铁固体加入到相同体积的下列溶液:①蒸馏水②0.1mol/L氢氧化钠③0.1mol/L氢氧化钡④0.1mol/L氯化铁,则铁离子浓度:④>①>②═③ |
分析 A、弱电解质的电离平衡常数是温度的函数;
B、PH=9的NaOH溶液和NH3•H2O溶液中,氢离子都是由水电离产生,而PH=9说明氢离子的浓度相等,所以水电离出的c(H+)相等;
C、常温下,混合液pH=5,c(H+)=1.0×10-5mol/L,则由Kw可知,c(OH-)=1.0×10-9mol/L,由电荷守恒可知,c(CH3COO-)-c(Na+)=c(H+)-c(OH-),据物料守恒:2c(Na+)=c(CH3COOH)+c(CH3COO-),据此分析;
D、氢氧化铁难溶于水,在水中的溶解度很小,一定温度下,溶液中Ksp[Fe(OH)3]=c(Fe3+)•c3(OH-)为定值,溶液中c(OH-)越大,c(Fe3+)越小.
解答 解:A、弱电解质的电离平衡常数是温度的函数,而加入少量NaOH固体使电离平衡逆向移动,但温度不变,所以c(OH-)•c(NH4+)/c(NH3•H2O)不变,故A错误;
B、PH=9的NaOH溶液和NH3•H2O溶液中,氢离子都是由水电离产生,而PH=9说明氢离子的浓度相等,所以水电离出的c(H+)相等,故B错误;
C、常温下,混合液pH=5,c(H+)=1.0×10-5mol/L,则由Kw可知,c(OH-)=1.0×10-9mol/L,由电荷守恒可知,Ⅰc(CH3COO-)-c(Na+)=c(H+)-c(OH-),据物料守恒:Ⅱ2c(Na+)=c(CH3COOH)+c(CH3COO-),Ⅰ×2+Ⅱ可得:c(CH3COO-)-c(CH3COOH)=2(c(H+)-c(OH-))=2×(10-5-10-9) mol/L,故C正确;
D、氢氧化铁难溶于水,在水中的溶解度很小,一定温度下,溶液中Ksp[Fe(OH)3]=c(Fe3+)•c3(OH-)为定值,溶液中c(OH-)越大,c(Fe3+)越小,当铁离子与氢氧根离子浓度相等时氢氧根离子浓度影响远大于铁离子,所以:①>④>②>③,故D错误;
故选C.
点评 本题主要考查了弱电解质的电离,关键是掌握弱电解质电离的影响因素,从而顺利地判断出电离平衡的移动方向.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯碱工业中,氢氧化钠在电解槽的阳极区产生 | |
| B. | 硫酸工业中,二氧化硫催化氧化使用催化剂,可增加二氧化硫的转化率 | |
| C. | 合成氨工业中,利用氨易液化,分离出N2、H2循环使用,可提高氨的产率 | |
| D. | 接触法制硫酸中三氧化硫用水吸收制成浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL0.4mol/L的甲酸中含甲酸的分子数为0.04NA | |
| B. | 在标准状态下,22.4L乙烷与乙烯的混合气体,含碳原子数为2NA | |
| C. | 18g水中含有的电子数为10NA | |
| D. | NA个23Na原子的质量为23g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol甲基中含有电子数为10NA | |
| B. | 常温下,1LpH=12的Na2CO3溶液中含有的OH-离子数为0.01 NA | |
| C. | 标准状况下,NO和O2各11.2L混合充分反应,所得气体的分子总数为0.75 NA | |
| D. | 50mL12mol•L-1盐酸和足量MnO2共热,转移的电子数为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 | c(CuCl2) | 实验现象 |
| I | 0.25mol/L | 有红色固体析出,有气泡冒出,一段时间内出气速率加快. |
| II | 2.00mol/L | 反应剧烈,有红色固体析出,产生大量气泡,有白色难溶物,试管外壁温度明显升高,一段时间内出气速率加快. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的大量排放会导致酸雨的形成 | |
| B. | 黄河三角洲的形成体现了胶体聚沉的性质 | |
| C. | 推广使用燃料电池汽车,可减少颗粒物、CO等有害物质的排放 | |
| D. | 轮船上挂锌锭防止铁腐蚀,属于牺牲阳极的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
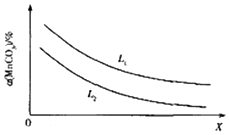 MnO2是常见的氧化剂、催化剂和活性电极材料.
MnO2是常见的氧化剂、催化剂和活性电极材料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com