
| ���� | ��״ | ��Է� ������ | �ܽ�� | |||
| ��ˮ | ��ˮ | �Ҵ� | ���� | |||
| ૼ�ȩ | ��ɫҺ�� | 96 | �� | ���� | ���� | ���� |
| ૼ״� | ��ɫҺ�� | 98 | ���� | ���� | ���� | ���� |
| ૼ��� | ��ɫ���� | 112 | �� | ���� | ���� | ���� |
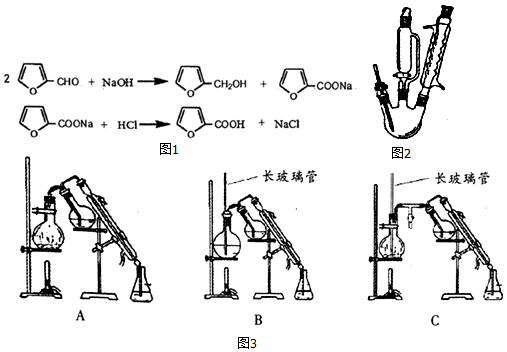
���� ��1�����������ڷ�Ӧ��ֿ��ǣ�
��2��ʵ������Ҫ����8-12�棬ѡ����ˮԡ��
��3�������ȡ�������ȡЧ����
��4������100mL 2��1ϡ���ᣬ��V��ˮ��=100mL��$\frac{2}{3}$��V�����ᣩ=100mL��$\frac{1}{3}$��ͬʱ���������ӷ�������������ʹ�øչ�����ֽ�ⶨ��ҺpH������ֽ������ɫʱ��˵�������������� ���ϲ���Һ�м����μ����ᣬ���������ǣ�˵�����������������
��5���������ѵ����ʷ������������ܼ����嵽�������ĵײ�������������ѹ̫��ʱ��ˮ�������Ų����������Ե�����ѹ�����ϵͳ����������ˮ���ӹܵ��Ͽ��������ʱӦ�����Բ����ƿ�ڵ����������¿��Ƿ��ѱ���������ˮ�����������볤��Բ����ƿ֮��Ӧװ��һ��T �ιܣ���T �ι��¶���һ�����ɼУ��Ա㼰ʱ��ȥ���������Ķ���ˮ�Σ�
��6������2ૼ�ȩ��ૼ��ᣬ�ɵ������ϵIJ�Ʒ�������ɴ˼�����ʣ�
��� �⣺��1���ɱ���֪��ૼ�ȩ����ˮ�������ֻ�ϼӿ췴Ӧ���ʣ�
�ʴ�Ϊ��ૼ�ȩ����ˮ�������ֻ�ϼӿ췴Ӧ���ʣ�
��2��ૼ�ȩ�ڼ��з�Ӧ�������ȣ�ʵ������Ҫ����8-12�棬����ˮԡ�ɽ��ͷ�Ӧ�ų���������
�ʴ�Ϊ����ˮԡ��
��3��50mL������ȡ��Һ������30mL������ȡ��Һ���ٷֱ���l0mL������ȡ���Σ�����������ȡҺ�ϲ�����ȥૼ״���Ч���Ϻã�
�ʴ�Ϊ��C��
��4������100mL 2��1ϡ���ᣬ��V��ˮ��=100mL��$\frac{2}{3}$��V�����ᣩ=100mL��$\frac{1}{3}$��ͬʱ���������ӷ���������������ˮ66mL������34mL������Ϊ������Ͳ�ֱ���ȡ66mlˮ��34mlŨ���ᣬ���ձ��л�ϣ��ò�����������ȣ�ʹ�øչ�����ֽ�ⶨ��ҺpH������ֽ������ɫʱ��˵�������������� ���ϲ���Һ�м����μ����ᣬ���������ǣ�˵�����������������
�ʴ�Ϊ������Ͳ�ֱ���ȡ66mlˮ��34mlŨ���ᣬ���ձ��л�ϣ��ò�����������ȣ�ʹ�øչ�����ֽ�ⶨ��ҺpH������ֽ������ɫʱ��˵�������������� ���ϲ���Һ�м����μ����ᣬ���������ǣ�˵�����������������
��5�������ӷ�����ȼ��Ӧ��ˮԡ�Ͻ��������м�ֱ��������ȣ��������ܼ����嵽�������ĵײ�������������ѹ̫��ʱ��ˮ�������Ų����������Ե�����ѹ�����ϵͳ����������ˮ���ӹܵ��Ͽ��������ʱӦ�����Բ����ƿ�ڵ����������¿��Ƿ��ѱ���������ˮ�����������볤��Բ����ƿ֮��Ӧװ��һ��T �ιܣ���T �ι��¶���һ�����ɼУ��Ա㼰ʱ��ȥ���������Ķ���ˮ�Σ���ѡ��C��
�ʴ�Ϊ����ˮԡ�Ͻ��������м�ֱ��������ȣ�C��
��6������2ૼ�ȩ��ૼ��ᣬ�����������ɵ�ૼ���Ϊ0.02mol������ૼ���IJ���Ϊ$\frac{1.5g}{0.02mol��112g/mol}$=67%��
�ʴ�Ϊ��67%��
���� ���⿼���л���ĺϳ�ʵ�飬�Ƕ�ѧ���ۺ������Ŀ��飬��Ҫѧ���߱���ʵ�Ļ�����ע��������������Լ�����Ŀ��Ϣ�Ļ�ȡ��ʹ�ã�������������ѧ���ݣ��ѶȽϴ�


 �����Ļ���������人������ϵ�д�
�����Ļ���������人������ϵ�д� ���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д� ��ٽ������½������������ϵ�д�
��ٽ������½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H1��0 | B�� | ��H2��0 | C�� | ��H1=��H3-2��H2 | D�� | 2��H4����H5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ʵ���Ũ��Ϊ0.5 mol/L��MgCl 2��Һ�У�������Cl - ����Ϊ N A | |
| B�� | 1mol�κ�����������Ϊ 22.4L | |
| C�� | 7.8gNa 2O 2�����������ӵ���Ŀ��0.1N A | |
| D�� | ��״���£�2.24Lˮ�к��еķ�����Ϊ0.1N A |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 20��ʱ��AgCl�����ڵ����ʵ���Ũ�ȵ�NaCl��MgCl2��Һ�е��ܶȻ���ͬ | |
| B�� | Ũ��Ϊ0.2mol/L��KHCO3��Һ��c��H2CO3����c��CO32-�� | |
| C�� | a mol/LHCN��Һ��b mol/L NaOH��Һ�������Ϻ�������Һ��c��Na+����c��CN-������aһ������b | |
| D�� | �����£���0.1mol/L��NaOH��Һ�У���ˮ�������c��H+����$\sqrt{{K}_{W}}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 �� | B�� | 2 �� | C�� | 3 �� | D�� | 4 �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
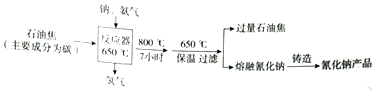

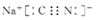 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ȡ̼���ƾ��壨Na2CO3•10H2O��100g������0.5mol/L��Na2CO3��Һ1000mL | |
| B�� | ����NH3NO3��Һ�����ձ����ܽ������ע������ƿ����������������ĸ������ | |
| C�� | ���ݺ�����ƿ���ȣ�����ʱ����Һ����ڿ̶��ߣ������ּ�������ˮ���̶��� | |
| D�� | ����ƿ������ˮϴ����δ��������������������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ϩ����ʹ����KMnO4��Һ��ɫ | |
| B�� | ����ȼ�ջ�����CO2����˲����������Դ | |
| C�� | ��ױ��е�������Ũ��ˮ�������ã���Һ�ֲ㣬�ϲ�ʳȺ�ɫ���²㼸����ɫ����֪�ױ�����ˮ����ȡ����Ӧ��ʹ��ˮ��ɫ | |
| D�� | ˮú�����ѽ�������¯������Ȼ�����ǻ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com