
| A.赤铁矿的主要成分是Fe3O4 |
| B.钢铁在湿空气中生锈,生成Fe2O3和H2 |
| C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加铁粉,然后过滤 |
| D.Fe3+与KSCN反应产生红色沉淀 |
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源:不详 题型:填空题
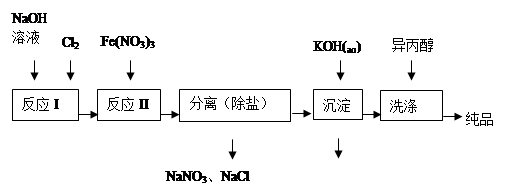
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 xH2O)。有如下操作:
xH2O)。有如下操作: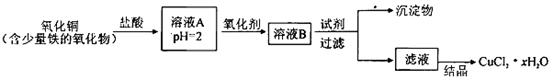
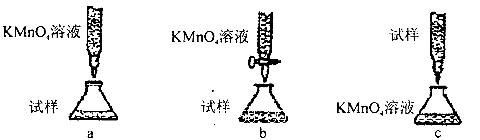
 xH2O)中的x值,某学生设计了两种实验方案:
xH2O)中的x值,某学生设计了两种实验方案:查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
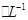 ,则此溶液最多能溶解铁粉的质量为
,则此溶液最多能溶解铁粉的质量为| A.5.6g | B.11.2 g | C.22.4g | D.33.6g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.增加钢材的硬度 | B.增强钢材的抗腐蚀能力 |
| C.使钢材美观 | D.增加钢材的韧性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 编号 | 实践操作 | 实验主要现象 | 离子方程式 |
| ① | 加入过量铁粉 | | |
| ② | 加入少量Na2O2粉末 | | |
| ③ | 加入少量AgNO3溶液 | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①② | B.②③ | C.③④ | D.①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com