
����Ŀ������ԭCO2�ǽ������ЧӦ����Դ�������Ҫ�ֶ�֮һ���о���������Cu/ZnO���������£�CO2��H2�ɷ�������ƽ�з�Ӧ���ֱ�����CH3OH��CO����Ӧ���Ȼ�ѧ����ʽ���£�
CO2��g��+3H2��g��CH3OH��g��+H2O��g����H1=��53.7kJmol��1 ��
CO2��g��+H2��g��CO��g��+H2O��g����H2 ��
ijʵ���ҿ���CO2��H2��ʼͶ�ϱ�Ϊ1��2.2������ͬѹǿ�£�������ͬ��Ӧʱ��������ʵ�����ݣ�
T��K�� | ���� | CO2ת���ʣ�%�� | �״�ѡ���ԣ�%�� |
543 | Cat.1 | 12.3 | 42.3 |
543 | Cat.2 | 10.9 | 72.7 |
553 | Cat.1 | 15.3 | 39.1 |
553 | Cat.2 | 12.0 | 71.6 |
[��ע]Cat.1��Cu/ZnO���װ���Cat.2��Cu/ZnO����Ƭ���״�ѡ���ԣ�ת����CO2�����ɼ״��İٷֱ�
��֪����CO��H2�ı�ȼ���ȷֱ�Ϊ��283.0kJmol��1�ͩ�285.8kJmol��1 ��
��H2O��1���TH2O��g����H3=44.0kJmol��1
��ش𣨲������¶ȶԡ�H��Ӱ�죩��
��1����ӦI��ƽ�ⳣ������ʽK=����Ӧ��ġ�H2=kJmol��1 ��
��2�����������CO2ת��ΪCH3OHƽ��ת���ʵĴ�ʩ�� ��
A.ʹ�ô���Cat.1
B.ʹ�ô���Cat.2
C.���ͷ�Ӧ�¶�
D.Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ��
E.���� CO2��H2�ij�ʼͶ�ϱ�
��3������ʵ�����ݱ���������ͬ�¶��²�ͬ�Ĵ�����CO2ת����CH3OH��ѡ������������Ӱ�죬��ԭ���� ��
��4������ͼ�зֱ���ӦI����������Cat.1����Cat.2��������¡���Ӧ���̩�������ʾ��ͼ��
��5���о�֤ʵ��CO2Ҳ��������ˮ��Һ��ͨ��������ɼ״��������ɼ״��ķ�Ӧ�����������õ缫��Ӧʽ�� ��
���𰸡�
��1��![]() ��+41.2
��+41.2
��2��C,D
��3���������ݱ�����ʱδ�ﵽƽ�⣬��ͬ�Ĵ����Է�Ӧ��Ĵ�������ͬ������ٸ�ʱ���¶Լ״�ѡ������Ӱ��
��4��

��5������CO2+6H++6e��=CH3OH+H2O
����������1��ƽ�ⳣ��Ϊ������Ũ����֮���뷴Ӧ��Ũ����֮���ı�ֵ. ��֪��CO��H2�ı�ȼ���ȷֱ�Ϊ��283.0kJmol��1�ͩ�285.8kJmol��1 �� ��H2O��1���TH2O��g����H3=44.0kJmol��1 �� ��֪�Ȼ�ѧ����ʽa��CO��g��+ ![]() O2��g��=CO2��g����H=��283.0kJmol��1 �� b��H2��g��+
O2��g��=CO2��g����H=��283.0kJmol��1 �� b��H2��g��+ ![]() O2��g��=H2O��1����H=��285.8kJmol��1 �� c��H2O��1���TH2O��g����H3=44.0kJmol��1 ��
O2��g��=H2O��1����H=��285.8kJmol��1 �� c��H2O��1���TH2O��g����H3=44.0kJmol��1 ��
�ɸ�˹���ɽ�b��a+c�ɵ�CO2��g��+H2��g��CO��g��+H2O��g����H2 =����285.8+283.0+44��kJmol��1=+41.2kJmol��1 ��
���Դ��ǣ� ![]() ��+41.2��
��+41.2��
��2��A��ʹ�ô���Cat.1��ƽ�ⲻ�ƶ����������ת���ʣ���A����
B��ʹ�ô���Cat.2���������ת���ʣ���B����
C�����ͷ�Ӧ�¶ȣ�ƽ�������ƶ���������ת���ʣ���C��ȷ��
D��Ͷ�ϱȲ��䣬���ӷ�Ӧ���Ũ�ȣ��������ƶ���������ת���ʣ���D��ȷ��
E������ CO2��H2�ij�ʼͶ�ϱȣ�������������ת���ʣ�������̼��ת���ʼ�С����E����
���Դ��ǣ�CD��
��3���ӱ������ݷ���������ͬ�¶��£���ͬ�Ĵ���������̼��ת���ʲ�ͬ��˵����ͬ�Ĵ����Ĵ�������ͬ����ͬ�Ĵ�����ͬ���¶ȣ�������̼��ת���ʲ�ͬ�����¶ȸߵ�ת���ʴ���Ϊ����ӦΪ���ȷ�Ӧ��˵������������δ�ﵽƽ������.
���Դ��ǣ��������ݱ�����ʱδ�ﵽƽ�⣬��ͬ�Ĵ����Է�Ӧ��Ĵ�������ͬ������ٸ�ʱ���¶Լ״�ѡ������Ӱ�죻
��4���ӱ������ݷ������ڴ���Cat.2�������£��״���ѡ���Ը���˵������Cat.2�Է�Ӧ���Ч�����ã������ܽ��ͷ�Ӧ�Ļ�ܣ�˵��ʹ�ô���Cat.2�ķ�Ӧ�����л�ܸ��ͣ����Դ��ǣ� 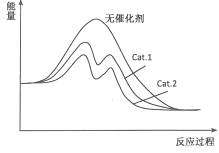 ��
��
��5��CO2Ҳ��������ˮ��Һ��ͨ��������ɼ״���CԪ�ػ��ϼ۽��ͣ�����ԭ��ӦΪ���ص�������Ӧ��
���Դ��ǣ�����CO2+6H++6e��=CH3OH+H2O��
�����㾫����������Ĺؼ��������⻯ѧƽ��״̬���ʼ����������֪ʶ�����ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч�����Լ��Ի�ѧƽ��ļ�������⣬�˽ⷴӦ��ת����=ת��Ũ�ȡ���ʼŨ�ȡ�100%=ת�����ʵ�������ʼ���ʵ�����100%����Ʒ�IJ���=ʵ�����ɲ�������ʵ����������Ͽɵõ���������ʵ�����100%��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�߷��ӻ�����R�Ľṹ��ʽ��ͼ�������й�R��˵����ȷ����

A. R�ĵ���֮һ�ķ���ʽΪC9H10O2
B. R��ȫˮ����������ΪС�����л���
C. ���������£�1molR��ȫˮ������NaOH�����ʵ���Ϊ2mol
D. ͨ���Ӿ۷�Ӧ�����۷�Ӧ��������R
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ȱ���ͬ���칹�������֣��Ӷ�������֪���ȱ���ͬ���칹����Ŀ��( )
A. 1 B. 2 C. 3 D. 4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ֪ʶ�ش��������⣮
��1��0.5molCH4�к�����������ӣ������ӵ�������NA��ʾ�����ڱ�״���µ����Ϊ L��0.1molH2SO4�к� molHԭ�ӣ�����ˮ���100mLˮ��Һ��c��H+��= ��
��2���ڷ�Ӧ3Zn+2Fe3+�T3Zn2++2Fe�У�Fe3+�������������ԭ��������1molZn��ȫ��Ӧת�Ƶĵ�����Ϊ mol��
��3��ѡ������ʵ�鷽���������ʣ������뷽����������ں����ϣ���ѡ����
A����ȡ��Һ B������ C���ᾧ D����Һ E������ F������
�ٷ�������л��е���ɳ �� �ڷ�����ˮ�Ļ���� ��
�۷���ˮ�����͵Ļ���� �� �ܷ���ƾ���ˮ�Ļ���� ��
��4���������������ʢ�CaO��SO3��SO2��P2O5 ��HNO3��H2SO4��HCl��NaCl��KClO3��KCl��KMnO4��HgO�����о���һ����������������������ʲ�ͬ�����������ʷֱ��ǣ����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������һ�����ʵ���Ũ�ȵ���Һ�Ǹ��л�ѧһ����Ҫʵ�飮ʵ����Ҫ����1mol/L��ϡ������Һ100mL���ش������й����⣺
��1������ʱ�������õ����������е� �� 
��2������ʱ�����õ������������ε����÷ֱ����� ��
��3������ʱ����ȷ�IJ���˳���ǣ�����ĸ��ʾ��ÿ����ĸֻ����һ�Σ���A����30mLˮϴ���ձ�2��3�Σ�ϴ��Һ��ע������ƿ
B����һ��������Ͳȷ��ȡ����Ũ��������������ע��ˮ�У��ò���������������ʹ�����ܽ�
C��������ȴ����Һ�ز�����ע��100mL������ƿ��
D��������ƿ�ǽ���ҡ��
E�����ý�ͷ�ιܼ�ˮ��ʹ��Һ����ǡ����̶�����
F������������ƿ��С�ļ�ˮ��ֱ��Һ��ӽ��̶�1��2cm��
��4�����ƹ����г������������ʹ������ҺŨ��ƫ�͵���������ţ�����û��ϴ���ձ��Ͳ��������������ˮ�����˿̶��ߣ�ȡ��ˮʹҺ��ǡ�õ��̶��ߣ�������ƿû�и���ܶ���ʱ���ӿ̶��ߣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������X��һ���л��ϳ��м��壬Z�dz����ĸ߷��ӻ����ij�о�С���������·�ߺϳ�X��Z��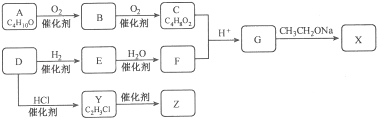
��֪���ٻ�����A�Ľṹ����2����
��RCOOR��+R��CH2COOR�� ![]()
![]()
��ش�
��1��д��������E�Ľṹ��ʽ �� F�й����ŵ���������
��2��Y��Z�Ļ�ѧ����ʽ����
��3��G��X�Ļ�ѧ����ʽ�� �� ��Ӧ��������
��4����C�л���B�����û�ѧ��������B�Ĵ��ڣ�Ҫ��д������������ͽ��ۣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�Na2CO3��NaHCO3������������ǣ� ��
A.Na2CO3���������ת��ΪNaHCO3
B.��ˮ�е��ܽ��Na2CO3��NaHCO3��
C.NaHCO3����Ca��OH��2��Һ��Ӧ����Na2CO3����
D.��ͬŨ�ȵ����ᷴӦʱ��NaHCO3��Na2CO3����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���мס�����λͬѧ��������ԭ��ط�Ӧ�������Ļ��˳�����˾�ʹ��þƬ����Ƭ���缫������ͬѧ���缫����6molL��1 H2SO4��Һ�У���ͬѧ���缫����6molL��1��NaOH��Һ�У���ͼ��ʾ��
��ش�
��1��д���׳��������ĵ缫��Ӧʽ�� ��
��2��д���ҳ��и����ĵ缫��Ӧʽ���ܷ�Ӧ�����ӷ���ʽ������ �� �ܷ�Ӧ�����ӷ���ʽΪ ��
��3���ɴ�ʵ�飬�ɵõ�������Щ��ȷ���ۣ�����д��ĸ��ţ���a������ԭ��ط�Ӧ�жϽ������˳��ʱӦע��ѡ����ʵĽ���
b��þ�Ľ����Բ�һ�������Ľ�����ǿ
c����ʵ��˵���������˳���ѹ�ʱ����û��ʵ�ü�ֵ
d����ʵ��˵����ѧ�о������ӣ���Ӧ������Ӱ��ϴ����Ӧ��������������
��4������ʵ��Ҳ������֤���ˡ�ֱ�����ý������˳���ж�ԭ����е�����������������������ɿ������ɿ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ��CuFeS2�������ֺ���ͭ����Ҫԭ�ϣ��ڸ�������������������������������ͭ��������������������ͭ���Ǻ�ɫ��ĩ�����������ϣ�ijѧУ��ѧ��ȤС��ͨ��ʵ����̽������ɫ��ĩ��Fe2O3��Cu2O�����ߵĻ���̽���������£�[��������]Cu2O����ϡ��������Cu��CuSO4 �� �ڿ����м�������CuO��
[�������]����1����ɫ��ĩ��Fe2O3 ��
����2����ɫ��ĩ��Cu2O��
����3����ɫ��ĩ��Fe2O3��Cu2O�Ļ���
[���̽��ʵ��]ȡ������ĩ��������ϡ�����У���������Һ���ٵμ�KSCN�Լ���
��1��������1��������ʵ�������� ��
��2���μ�KSCN�Լ�����Һ�����ɫ��ijͬѧ��Ϊԭ�����ĩ��һ����������������������Ϊ����˵�������� �� ����������ɣ�����Ҫд����Ӧ�Ļ�ѧ����ʽ�� ��
��3���������ĩ��ȫ��Һ������ڣ��μ�KSCN�Լ�ʱ��Һ�����ɫ����֤��ԭ�����ĩ�� �� д��������������ԭ��Ӧ�����ӷ���ʽ�� ��
��4��[̽������]�����������ȷ����ɫ��ĩΪFe2O3��Cu2O�Ļ���ʵ��С���ȡ3.04g�ú�ɫ��ĩ���������ʵ�鷽������ʵ�飮�������ϵ�֪������Һ��ͨ��������Һ������Զ�ʹCu2+��Fe2+��Fe3+�ֱ����ɳ�����pH���£�
���� | Cu��OH��2 | Fe��OH��2 | Fe��OH��3 |
��ʼ����ʱ��pH | 6.0 | 7.5 | 1.4 |
������ȫʱ��pH | 13 | 14 | 3.7 |
�����3.04g��ɫ��ĩ��������ϡ�����У��ټ�������H2O2��Һ�����ó�������ҺX��
���������ҺX�м�������Cu��OH��2��ĩ��������ҺpH=4.0�����ˣ��ú��ɫ����Y����ҺZ��
���������Y������գ���1.6g��ɫ����M��
�����������ҺZ����Ũ������ȴ�ᾧ�����ˣ���6.0gCuSO45H2O���壮
�ٳ���Y�Ļ�ѧʽΪ ��
�ڲ�����в���Ҫ�õ���ʵ������ ��
a���ձ�b��������c����Һ©��d���ƾ���e������̨������Ȧ��f��������ƽg����Ͳh��������i������ƿ��
�ۺ�ɫ��ĩ��Ʒ��Cu2O����������Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com