
【题目】已知A是芳香烃,苯环上只有一个取代基,A完全加氢后分子中有两个甲基,E的分子式为C9H8O2,能使溴的四氯化碳溶液褪色,其可以用来合成新型药物H,合成路线如图所示。

已知:
①
②
请回答下列问题:
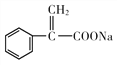
(1)写出有机物A的结构简式:____________。有机物H中存在的官能团名称为_______________。
(2)上述反应过程中属于取代反应的有________________(填序号)。
(3)有机物D在一定条件下可以聚合形成高分子,写出该聚合反应的化学方程式_____________________。
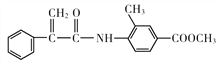
(4)写出H在氢氧化钠催化作用下的水解方程式:_________________________。
(5)有机物E有多种同分异构体,写出符合下列条件的同分异构体的结构简式:________________。
A.存在苯环且苯环上核磁共振氢谱只有2组峰值B.能发生银镜反应C.能发生水解反应
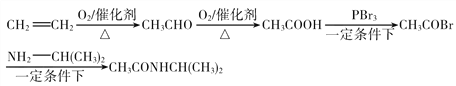
(6)参照H的上述合成路线,设计一条由乙烯和NH2—CH(CH3)2为起始原料制备医药中间体CH3CONHCH(CH3)2的合成路线:_________(需注明反应条件)
【答案】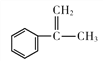 碳碳双键、肽键、酯基 ②⑤⑥
碳碳双键、肽键、酯基 ②⑤⑥ 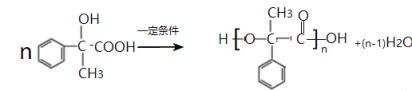
 +2NaOH→CH3OH+
+2NaOH→CH3OH+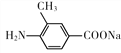 +
+
![]()
【解析】
A是芳香烃,根据分子式含有1个苯环,能和溴的四氯化碳溶液发生反应,说明含有碳碳双键,A和氢气发生加成反应后有两个甲基,说明含有烃基上含有1个支链,即A的结构简式为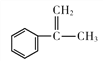 ,和溴的四氯化碳溶液发生加成反应,即B的结构简式为
,和溴的四氯化碳溶液发生加成反应,即B的结构简式为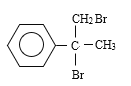 ,反应②发生卤代烃的水解反应,羟基取代溴原子的位置,即C的结构简式为
,反应②发生卤代烃的水解反应,羟基取代溴原子的位置,即C的结构简式为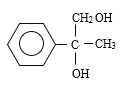 ,C转化D发生氧化反应,D的结构简式为:
,C转化D发生氧化反应,D的结构简式为: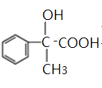 ,对比D和E的分子式,以及E能使溴的四氯化碳溶液褪色,反应④发生消去反应,即E的结构简式为:
,对比D和E的分子式,以及E能使溴的四氯化碳溶液褪色,反应④发生消去反应,即E的结构简式为: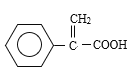 ,根据信息①,溴原子取代羧基中羟基的位置,F的结构简式为:
,根据信息①,溴原子取代羧基中羟基的位置,F的结构简式为: ,根据信息②发生取代反应,即H的结构简式为:
,根据信息②发生取代反应,即H的结构简式为: 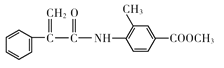 ;
;
A是芳香烃,根据分子式含有1个苯环,能和溴的四氯化碳溶液发生反应,说明含有碳碳双键,A和氢气发生加成反应后有两个甲基,说明含有烃基上含有1个支链,即A的结构简式为 ,和溴的四氯化碳溶液发生加成反应,即B的结构简式为
,和溴的四氯化碳溶液发生加成反应,即B的结构简式为 ,反应②发生卤代烃的水解反应,羟基取代溴原子的位置,即C的结构简式为
,反应②发生卤代烃的水解反应,羟基取代溴原子的位置,即C的结构简式为 ,C转化D发生氧化反应,D的结构简式为:
,C转化D发生氧化反应,D的结构简式为: ,对比D和E的分子式,以及E能使溴的四氯化碳溶液褪色,反应④发生消去反应,即E的结构简式为:
,对比D和E的分子式,以及E能使溴的四氯化碳溶液褪色,反应④发生消去反应,即E的结构简式为: ,根据信息①,溴原子取代羧基中羟基的位置,F的结构简式为:
,根据信息①,溴原子取代羧基中羟基的位置,F的结构简式为: ,根据信息②发生取代反应,即H的结构简式为:
,根据信息②发生取代反应,即H的结构简式为:  ;
;
(1)根据上述分析,A的结构简式为 ;依据H的结构简式,含有的官能团为碳碳双键、肽键、酯基;
;依据H的结构简式,含有的官能团为碳碳双键、肽键、酯基;
(2)属于取代反应的是②⑤⑥;
(3)根据有机物D的结构简式,通过缩聚反应形成高分子化合物,其化学反应方程式为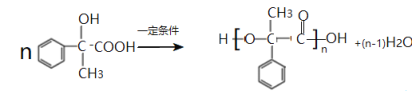 ;
;
(4)H中含有肽键和酯基,在氢氧化钠条件下发生水解反应的方程式为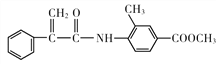 +2NaOH→CH3OH+
+2NaOH→CH3OH+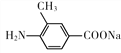 +
+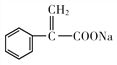 ;
;
(5)A、存在苯环,核磁共振氢谱有2组峰,推出是对称结构;B、能发生银镜反应,推出含有醛基;C、能发生水解反应,含有酯基,符合条件的同分异构体为![]() ;
;
(6)根据中间体的结构简式,生成中间体两种有机物分别是:CH3COBr和(CH3)2CHNH2,由CH3COOH和PBr3发生取代反应生成CH3COBr,乙酸由乙醛氧化生成,乙醛可以由乙烯直接转化成,也可以由乙醇氧化生成,乙醇由乙烯的水化法产生,选择最简单的路线,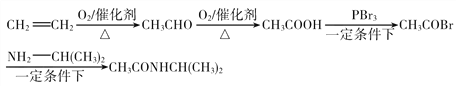 。
。


 互动英语系列答案
互动英语系列答案科目:高中化学 来源: 题型:
【题目】次氯酸溶液是常用的消毒剂、漂白剂。某学习小组根据需要欲制备浓度不小于0.8mol/L的次氯酸溶液。
(查阅资料)资料1:常温常压下,Cl2O为棕黄色气体,沸点为3.8 ℃,42 ℃以上会分解生成Cl2和O2,Cl2O易溶于水并与水立即反应生成HClO。
资料2:将氯气和空气(不参与反应)按体积比1∶3混合通入潮湿的碳酸钠中发生反应2Cl2+2Na2CO3+H2O=Cl2O+2NaCl+2NaHCO3,用水吸收Cl2O(不含Cl2)制得次氯酸溶液。
(装置及实验)用以下装置制备次氯酸溶液

回答下列问题:
(1)各装置的连接顺序为____→_____→_____→____→E;
(2)装置 A 中反应的离子方程式是__________________;
(3)装置 E中反应的化学方程式是_____________________;
(4)装置 B 中多孔球泡和搅拌棒的作用是____,反应过程中,装置B需放在冷水中,其目的是____。
(5)装置C的主要作用是_____________________;
(6)此方法相对于用氯气直接溶于水制备次氯酸溶液的优点是(答出一条即可)______________。
(7)若装置B中生成的Cl2O气体有20%滞留在E前各装置中,其余均溶于装置E的水中,装置E所得500mL次氯酸溶液浓度为0.8mol/L,则至少需要含水8%的碳酸钠的质量为___g。
(8)配平下列离子方程式:______Fe(OH)3+ ClO![]() + OH
+ OH![]() — FeO42-+ Cl-+ H2O。
— FeO42-+ Cl-+ H2O。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )

A. 图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则等物质的量浓度的NaA和NaB混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
B. 图2中在b点对应温度下,将pH=2的H2SO4溶液与pH=12的NaOH溶液等体积混合后,溶液显中性
C. 用0.0100 mol/L硝酸银标准溶液,滴定浓度均为0.1000 mol/L Cl-、Br-及I-的混合溶液,由图3曲线,可确定首先沉淀的是Cl-
D. 图4表示在N2(g)+3H2(g) ![]() 2NH3(g)达到平衡后,减小NH3浓度时速率的变化
2NH3(g)达到平衡后,减小NH3浓度时速率的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业生产苯乙烯是利用乙苯的脱氢反应:![]() +H2(正反应吸热),下列说法正确的是
+H2(正反应吸热),下列说法正确的是
A. 乙苯、苯乙烯都能够发生氧化反应和还原反应
B. 苯乙烯中所有原子一定共平面
C. 平衡后,在恒温恒容条件下,再充入乙苯,平衡正向移动,平衡常数增大
D. 苯、乙苯的主要来源是石油的分馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图装置进行实验,下列推断正确的是
选项 | I中试剂 | II中试剂及现象 | 推 断 |
A | 铁粉与湿棉花 | 肥皂水冒泡 | 铁粉与水蒸气 发生了反应 |
B | 硫酸亚铁 | 品红溶液褪色 | FeSO4分解生成 FeO和SO2 |
C | 涂有石蜡油的碎瓷片 | 酸性高锰酸钾溶液 褪色 | 石蜡油分解产物中 含有不饱和烃 |
D | 氯化铵 | 酚酞溶液不变红色 | 氯化铵不分解 |

A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体说法的正确组合是

①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、NaF、NaCl、H2O、H2S晶体的熔点依次降低
④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-紧邻
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠熔化时离子键被破坏
A.①②③⑥ B.①②④
C.③⑤⑦ D.③⑤⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二异丙烯基苯是工业上常用的交联剂,可用于制备高性能超分子聚合物,其结构如下图所示。下列有关二异丙烯基苯的说法错误的是

A. 在催化剂存在下可发生加聚反应
B. 与溴水混合后加入铁粉可发生取代反应
C. 分子中所有碳原子可能都处于同一平面
D. 其一氯代物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素。其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大。P元素的第三电子层处于全充满状态,第四电子层只有一个电子。请回答下列问题:
(1)基态X的外围电子电子排布图为_____,P元素属于_____ 区元素。
(2)XZ2分子的空间构型是_____,YZ2分子中Y的杂化轨道类型为_____,相同条件下两者在水中的溶解度较大的是_____(写分子式),理由是_____。
(3)含有元素N的盐的焰色反应为____色,许多金属盐都可以发生焰色反应,其原因是___。
(4)元素M与元素Q形成晶体中,M离子与Q离子的配位数之比为_____。
(5)P单质形成的晶体中,P原子采取的堆积方式为_____,P原子采取这种堆积方式的空间利用率为_____(用含π表达式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com