
【题目】I.已知:键能指在标准状况下,将 1mol 气态分子 AB(g)解离为气态原子 A(g),B(g)所需的能量,用符号 E 表示,单位为 kJ/mol。N≡N的键能为 946 kJ/mol,H-H 的键能为 436 kJ/mol,N-H 的键能为 391 kJ/mol,则生成 2 mol NH3 过程中______(填“吸收”或“放出”)的能量为______。
II.(1)下列装置属于原电池的是 ______;
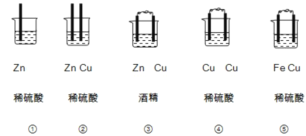
(2)在选出的原电池中,______是负极,发生______反应,正极的现象______;
(3)此原电池反应的化学方程式为______。
(4)将 CH4设计成燃料电池, 其利用率更高, 装置如图所示( A、B 为多孔碳棒), 电池总反应为:CH4+2O2+2KOH=K2CO3+3H2O。
①实验测得 OH-定向移向 B 电极,则_______处电极入口通甲烷(填 A 或 B)。
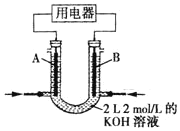
②当消耗甲烷的体积为 33.6L(标准状况下)时,假设电池的能量转化率为 80%,则导线中转移电子的物质的量为_______。
【答案】放出 92kJ ⑤ Fe 氧化 有气泡产生 Fe+H2SO4=FeSO4+H2↑ B 9.6mol
【解析】
Ⅰ.已知N≡N的键能为946kJ/mol,H-H的键能为436kJ/mol,N-H的键能为39 1kJ/mol,根据N2 +3H2![]() 2NH3,反应的△H=(946kJ/mol+3×436kJ/mol)-6×391kJ/mol=-92 kJ/mol,因此生成2molNH3过程中的热量变化为92kJ,该反应为放热反应,故答案为:放出;92kJ;
2NH3,反应的△H=(946kJ/mol+3×436kJ/mol)-6×391kJ/mol=-92 kJ/mol,因此生成2molNH3过程中的热量变化为92kJ,该反应为放热反应,故答案为:放出;92kJ;
Ⅱ(1)①中没有两个活泼性不同的电极,所以不能构成原电池;
②没有构成闭合回路,所以不能构成原电池;
③酒精为非电解质溶液,所以不能构成原电池;
④两材料相同,所以不能构成原电池;
⑤符合原电池的构成条件,所以能构成原电池;
故答案为:⑤;
(2)该装置中,铁易失电子而作负极,铜作正极,负极上铁失电子发生氧化反应生成亚铁离子,正极上氢离子得电子发生还原反应而生成氢气,所以有气泡生成,故答案为:Fe;氧化;有气泡产生;
(3)该原电池中,负极上铁失电子生成亚铁离子,正极上氢离子得电子生成氢气,所以电池反应式为:Fe+H2SO4=FeSO4+H2↑,故答案为Fe+H2SO4=FeSO4+H2↑;
(4)①实验测得OH-定向移向B电极,原电池中阴离子向负极移动,则B电极是负极,因此B处电极入口通甲烷,故答案为:B;
②负极的电极反应式为CH4-8e-+10OH-=CO32-+7H2O,当消耗的甲烷体积为33.6L(标准状况下),则物质的量是1.5mol,假设电池的能量转化率为80%,则导线中转移电子的物质的量为1.5mol×80%×8=9.6mol,故答案为:9.6mol。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。据此下列说法正确的是

A. 该硫酸的物质的量浓度为9.2mo1/L
B. 该硫酸与等体积的水混合所得溶液的质量分数为49%
C. 配制250mL 4.6mo1/L的稀硫酸需取该硫酸62.5mL
D. 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2mo1/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳整理是科学学习的重要方法之一。氧族元素的各种性质可归纳整理为如下表所示的表格(部分)。
8O | 16S | 34Se | 52Te | |
单质熔点(℃) | -218.4 | 113 | 450 | |
单质沸点(℃) | -183 | 444.6 | 685 | 989 |
主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
原子半径 | 逐渐增大 | |||
单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
请根据表回答下列问题:
(1)硒的熔点范围可能是___________。
(2)碲的化合价可能有__________。
(3)氢硒酸有较强的________(填“氧化性”或“还原性”),因此放在空气中长期保存易变质,其可能发生反应的化学方程式为_______________。
(4)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:______Al2Te3+______=____Al(OH)3+______H2Te↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,2.24 LCH3OH中含有的原子数目为6 NA
B. 18 g 2H2O中含有的电子数目为10 NA
C. 25℃时,1 L pH=13的Ba(OH)2溶液中含有OH-数为0.05 NA
D. 常温下,21 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. H2和D2互为同位素
B. 分子式为C2H6O、C4H10的有机物均有两种同分异构体
C.  的名称是2-乙基丁烷
的名称是2-乙基丁烷
D. 12C原子是指质子数为6,中子数是12的一种核素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温条件下,Al和Fe3O4反应生成Fe和Al2O3。下列说法正确的是

A.该反应过程中的能量变化如图所示
B.该反应条件下,Al的还原性弱于Fe
C.实验室进行该反应时常加入KClO3作催化剂
D.1molFe3O4参与反应转移8×6.02×1023个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应aA(g)+bB(g)![]() cC(g) ΔH,在密闭容器中进行。如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况。下列推断中正确的是
cC(g) ΔH,在密闭容器中进行。如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况。下列推断中正确的是
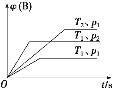
A. p1<p2,T1>T2,a+b<c,ΔH>0
B. p1<p2,T1>T2,a+b>c,ΔH>0
C. p1>p2,T1<T2,a+b<c,ΔH<0
D. p1>p2,T1<T2,a+b>c,ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取软锰矿石(主要成分为MnO2)116g 跟足量浓盐酸发生如下反应(杂质不参与反应)MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,制得22.4L Cl2(标准状况)。下列有关说法中不正确的是
MnCl2+Cl2↑+2H2O,制得22.4L Cl2(标准状况)。下列有关说法中不正确的是
A.这种软锰矿石中MnO2的质量分数为75%
B.被氧化的HCl的物质的量为4mol
C.参加反应的HCl的质量为146g
D.被还原的MnO2的物质的量为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五氧化二碘(I2O5)可用作氧化剂,除去空气中的一氧化碳,易溶于水形成碘酸,不溶于无水乙醇、乙醚、氯仿和二硫化碳。用下列装置制备五氧化二碘(加热装置及夹持装置省略)。

制备五氧化二碘的步骤如下:
步骤1:I2与KClO3按一定比例加入反应器M中,用硝酸调节pH=1~2,温度控制在80~90℃,搅拌反应1h,使反应完全。
步骤2:然后冷却至室温,析出碘酸氢钾晶体。将过滤得到的晶体加水、加热溶解,并用足量氢氧化钾溶液中和至溶液pH为10。再冷却结晶,过滤得到的晶体于118℃干燥3h,得到碘酸钾产品。
步骤3:将步骤2制得的碘酸钾酸化后得碘酸(HIO3),再将碘酸在干燥空气气流中加热到200℃失水得到五氧化二碘。
(1)五氧化二碘可除去空气中的一氧化碳,反应生成碘单质,该反应中氧化剂与还原剂的物质的量之比为___。
(2)仪器M的名称是___。
(3)步骤1中除了生成碘酸氢钾[KH(IO3)2]外,同时还生成氯化钾和氯气,若n(KCl):n(C12)=5:3,写出该反应的化学方程式:___,该反应中的氧化剂是___(填化学式)。
(4)反扣的漏斗N除了可以防止倒吸,还有一个作用是____,NaOH溶液的作用是___。
(5)步骤2中的主要反应为KH(IO3)2+KOH===2KIO3+H2O,称取0.550g碘酸钾产品(假设杂质不参与反应),将产品放入烧杯中,加蒸馏水溶解,并加入足量酸化的KI溶液,配制成100mL溶液,取10.00mL配制的溶液于锥形瓶中并加入指示剂,然后用0.1mol·L-1 Na2S2O3标准溶液滴定至终点,三次实验平均消耗标准溶液的体积为15.00mL。(已知I2+2Na2S2O3=2NaI+Na2S4O6)
①该滴定选择的指示剂是_____。
②该碘酸钾产品中碘酸钾的质量分数是____%(保留三位有效数字)。
③若装Na2S2O3标准溶液的滴定管没有用Na2S2O3标准溶液润洗,则所测得产品的质量分数___(填“偏高”或“偏低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com