
【题目】下列生活中常见物质主要成分的化学式表示正确的是( )
A.铁红—Fe2O3B.漂白粉—NaClO
C.生石灰—Ca(OH)2D.纯碱—NaHCO3
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】根据所学知识,回答下列问题:
Ⅰ.在① ![]() ②
② ![]() ③
③ ![]() ④
④ ![]() ⑤
⑤![]() ⑥
⑥ ![]() 中:
中:
(1)____和____互为同位素。
(2)____和____质量数相等,但不能互称同位素。
(3)____和____的中子数相等,但质子数不相等,所以不是同一种元素。
Ⅱ.已知31 g白磷变为31 g红磷释放能量。试回答:
(1)上列变化属于_____________变化。
(2)31 g白磷具有的能量_________(填“>”或“<”,下同)31 g红磷具有的能量。
(3)31 g白磷完全燃烧释放的能量_________31 g红磷完全燃烧释放的能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:

已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1molD可与1mol NaOH或2mol Na反应。
回答下列问题:
(1)A的结构简式为____________。
(2)B的化学名称为____________。
(3)C与D反应生成E的化学方程式为____________。
(4)由E生成F的反应类型为____________。
(5)G是分子式为____________。
(6)L是D的同分异构体,可与FeCl3溶液发生显色反应,1mol的L可与2mol的Na2CO3反应,L共有______种;其中核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1的结构简式为___________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表得第_____________族,其基态原子中未成对电子的个数为______。
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为____________________,所含非金属元素的电负性由大到小的顺序是____________________。
(3)尿素分子中、碳原子为________杂化,分子中σ键与π键的数目之比为____________________。
(4)FeO晶体与NaCl晶体结构相似,比较FeO与NaCl的晶格能大小,还需要知道的数据是______。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为____________________。
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如下图所示,则该物质的化学式为____________________。若晶体密度为dg·cm3,则晶胞中最近的两个碳原子的距离为____________________pm(阿伏伽德罗常数的值用NA表示,写出简化后的计算式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果醋是一种由苹果发酵而形成的具有解毒、降脂、减肥等明显药效的健康食品。苹果酸(2-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为![]() 。下列相关说法不正确的是( )
。下列相关说法不正确的是( )
A. 苹果酸在一定条件下能发生催化氧化反应
B. 1 mol苹果酸与足量NaHCO3溶液反应消耗2 mol NaHCO3
C. 1 mol苹果酸与足量Na反应生成33.6 L H2(标准状况下)
D. 1 mol苹果酸分别和足量Na或NaOH反应消耗两者物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NaAlO2、Ba(OH)2、NaOH配成100.0 mL混合溶液,向该溶液中通入足量CO2,生成沉淀的物质的量n(沉淀),与通入CO2的体积(标准状况下)V(CO2)的关系,如下图所示,

下列说法中正确的是( )
A. P点的值为12.32
B. 混合溶液中c(NaOH)+c(NaAlO2)=4.0 mol/L
C. bc段的化学反应方程式为:NaOH+CO2=NaHCO3
D. cd段表示Al(OH)3沉淀溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的离子除了铜离子(Cu2+)外,自然界中还存在亚铜离子(Cu+)。Cu+在水溶液中没有Cu2+稳定,易在酸性条件下发生反应:2Cu+═Cu2++Cu。+1价铜的化合物通常是难溶物,如Cu2O、CuI、CuCl、Cu2S、等。
回答下列问题:
(1) 在新制Cu(OH)2悬浊液中滴入葡萄糖溶液,加热生成难溶物的颜色为________;若继续加热,出现黑色物质,判断这种物质的化学式为________________。
(2) 在CuCl2溶液中滴加过量KI溶液,可发生如下反应:
a.2Cu2++4I-═2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I-═2CuCl↓(白色)+I2
为顺利观察到CuI、CuCl白色沉淀,可以加入下列试剂中的________。
A.乙醇 B.苯 C.盐酸溶液 D.NaCl溶液
(3) Cu2S在稀H2SO4酸化下与氧气反应生成CuSO4,该反应的化学方程式为________________________________;该反应的还原剂为________________,当1 mol O2发生反应时,还原剂所失电子的物质的量为________mol,其中被S元素还原的O2的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W、M为短周期主族元素,25°C时,其最高价氧化物对应的水化物(浓度均为 0.01mol·L-1)溶液的pH和原子半径的关系如图所示。下列有关说法不正确的是

A. 最简单气态氢化物的热稳定性:Z>W
B. Y的最高价氧化物的电子式为:![]()
C. W的气态氢化物是强酸
D. X、M两种元素形成的简单离子半径大小顺序:X>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮化合物在材料方面的应用越来越广泛。
(1)甲胺(CH3NH2)是合成太阳能敏化剂的原料。工业合成甲胺原理:
CH3OH(g)+NH3(g)![]() CH3NH2(g)+H2O(g)△H。
CH3NH2(g)+H2O(g)△H。
①已知键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如下表所示:
化学键 | C-H | C-O | H-O | N-H | C-N |
键能/kJ·mol-1 | 413 | 351 | 463 | 393 | 293 |
则该合成反应的△H=______________。
②一定条件下,在体积相同的甲、乙、丙、丁四个容器中,起始投入物质如下:
NH3(g)/mol | CH3OH(g)/mol | 反应条件 | |
甲 | 1 | 1 | 498K,恒容 |
乙 | 1 | 1 | 598K,恒容 |
丙 | 1 | 1 | 598K,恒压 |
丁 | 2 | 3 | 598K,恒容 |
达到平衡时,甲、乙、丙、丁容器中的CH3OH转化率由大到小的顺序为_______________。
(2)工业上利用镓(Ga)与NH3在高温下合成固体半导体材料氮化镓(GaN),其反应原理为2Ga(s)+2NH3(g)![]() 2GaN(s)+3H2(g)△H=-30.81kJ·mol-1。
2GaN(s)+3H2(g)△H=-30.81kJ·mol-1。
①在密闭容器中充入一定量的Ga与NH3发生反应,实验测得反应体系与温度、压强的相关曲线如图所示。图中A点与C点的化学平衡常数分别为KA和KC,下列关系正确的是_________(填代号)。

a.纵轴a表示NH3的转化率 b.纵轴a表示NH3的体积分数 c.T1<T2 d.KA<Kc
②镓在元素周期表位于第四周期第ⅢA族,化学性质与铝相似。氮化镓性质稳定,不溶于水,但能缓慢溶解在热的NaOH溶液中,该反应的离子方程式为_____________________。
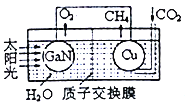
(3)用氮化镓与铜组成如图所示的人工光合系统,利用该装置成功地以CO2和H2O为原料合成CH4。铜电极表面发生的电极反应式为___________。两电极放出O2和CH4相同条件下的体积比为________,为提高该人工光合系统的工作效率,可向装置中加入少量的__________(填“盐酸”或“硫酸”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com