
| A. | 浓硫酸 | B. | 稀硫酸 | C. | 浓盐酸 | D. | 稀硝酸 |
科目:高中化学 来源: 题型:解答题
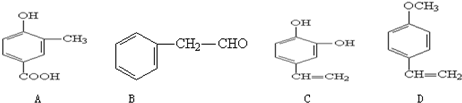
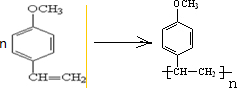
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 芝麻酱每100 g含有 蛋白质:19.2 g 脂肪:52.7 g 碳水化合物16.8 g 维生素 A:17 μg 铁:50.3 mg 硒:4 μg 含钙:相当于300 g豆腐 含铁:相当于800 g鸡蛋 (提醒:芝麻酱可引起部分婴儿过敏性皮炎) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用BaCl2溶液鉴别SO42- 和 SO32- | |
| B. | 用浓HNO3与Cu 反应制备NO2 | |
| C. | 用特殊方法把固体物质加工到纳米级(1nm-100nm) 的超细粉末粒子,制得纳米材料,纳米材料也是一种胶体 | |
| D. | 将混有HCl的Cl2通入饱和NaCl溶液中除去HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+HOCl→HOCH2-CH2Cl | |
| B. |  +HNO3$→_{△}^{浓硫酸}$ +HNO3$→_{△}^{浓硫酸}$ +H2O +H2O | |
| C. | 2CH3CH2OH+O2 $→_{△}^{Cu}$2CH3CHO+2H2O | |
| D. | C12H22O11+H2O $→_{△}^{稀H_{2}SO_{4}}$ C6H12O6+C6H12O6 蔗糖 葡萄糖 果糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加氢氧化钠溶液,加热,滴入酚酞试剂 | |
| B. | 加水,将湿润的红色石蕊试纸放在试管口 | |
| C. | 加氢氧化钠溶液,加热,滴入紫色石蕊试剂 | |
| D. | 加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
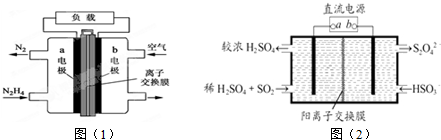
| A. | 图(1)中的a电极应与 图(2)的a相连 | |
| B. | 图(1)中a电极应的反应方程式为:N2H4+4OH--4e-═N2+4H2O | |
| C. | 用该燃料电池作为装置图(2)的直流电,吸收1 molSO2至少需要通人 0.5 mol N2H4 | |
| D. | 图(1)中OH-由阴离子交换膜从左流向右,图(2)中H+由阳离子交换膜从右流向左 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com