
【题目】金属镍在电池、合金、催化剂等方面应用广泛.
(1)下列关于金属及金属键的说法正确的是 .
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是 .
(3)过渡金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n= .CO与N2结构相似,CO分子内σ键与π键个数之比为 .
(4)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH).甲醇分子内C原子的杂化方式为 ,甲醇分子内的O﹣C﹣H键角 (填“大于”“等于”或“小于”)甲醛分子内的O﹣C﹣H键角.
【答案】(1)b;(2)C;(3)4;1:2;(4)sp3;小于.
【解析】试题分析:(1)金属键没有方向性和饱和性,金属键是金属阳离子和自由电子间的相互作用,金属导电是因为自由电子在外加电场作用下发生定向移动,属具有光泽是因为自由电子能够吸收可见光;
(2)Ni的外围电子排布为3d84s2,3d能级上有2个未成对电子;
(3)CO配位时,提供碳原子上的一对孤对电子;CO中C和O以三键结合;
(4)ABm型杂化类型的判断:
中心原子电子对计算公式:电子对数n=![]() (中心原子的价电子数+配位原子的成键电子数±电荷数)
(中心原子的价电子数+配位原子的成键电子数±电荷数)
注意:①当上述公式中电荷数为正值时取“﹣”,电荷数为负值时取“+”.
②当配位原子为氧原子或硫原子时,成键电子数为零.
根据n值判断杂化类型:一般有如下规律:当n=2,sp杂化;n=3,sp2杂化;n=4,sp3杂化;sp3杂化是四面体构型,sp2杂化,分子呈平面三角形.
解:(1)a.金属键没有方向性和饱和性,故A错误;
b.金属键是金属阳离子和自由电子间的相互作用,故B正确;
c.金属导电是因为自由电子在外加电场作用下发生定向移动,故C错误;
d.金属具有光泽是因为自由电子能够吸收可见光,故D错误,
故答案为:b;
(2)Ni的外围电子排布为3d84s2,3d能级上有2个未成对电子.第二周期中未成对电子数为2的元素有C、O,其中C的电负性小,
故答案为:C;
(3)中心原子价电子数与配体提供电子总数之和为18,中心原子是Ni,价电子排布3d84s2,共10个电子,CO配位时,提供碳原子上的一对孤对电子,![]() =4;CO中C和O以三键结合,含有1个σ键、2个π键,故答案为:4;1:2;
=4;CO中C和O以三键结合,含有1个σ键、2个π键,故答案为:4;1:2;
(4)甲醇分子内C的成键电子对数为4,无孤电子对,杂化类型为sp3,是四面体结构,甲醛分子中的碳采取sp2杂化,是平面三角形结构,甲醇分子内O﹣C﹣H键角比甲醛分子内O﹣C﹣H键角小,故答案为:sp3;小于.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案科目:高中化学 来源: 题型:
【题目】用FeS2纳米材料制成的高容量锂电池,电极分别是二硫化亚铁和金属锂,电解液是含锂盐的有机溶剂。下列说法错误的是
A. 金属锂作电池的负极
B. 电池正极反应为FeS2+4Li++4e-==Fe+2Li2S
C. 放电时,Li+向负极迁移
D. 电池总反应为FeS2+4Li ==Fe+2Li2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
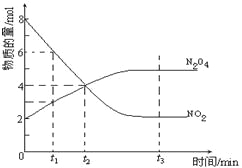
(1)在该温度下,反应的化学平衡常数表达式为:
(2)若t1=10s,t2=20s,计算从t1至t2时以N2O4表示的反应速率: molL﹣1s﹣1
(3)图中t1、t2、t3哪一个时刻表示反应已经达到平衡?答:
(4)t1时,正反应速率 (填“>”、“<”或“=”)逆反应速率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是四种短周期元素,E是过渡元素.A、B、C同周期,C、D同主族,A的原子结构示意图为:![]() ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
(1)写出下列元素的符号:A B C D
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是 ,碱性最强的是 .
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是 ,电负性最大的元素是 .
(4)D的氢化物比C的氢化物的沸点 (填“高“或“低“),原因
(5)E元素原子的核电荷数是 ,E元素在周期表的位置 .
(6)A、B、C最高价氧化物的晶体类型是分别是 晶体、 晶体、 晶体
(7)画出D原子的核外电子轨道表示式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知次氯酸分子的结构式为H﹣O﹣Cl,下列有关说法正确的是( )
A.该分子的电子式是H:O:Cl
B.O原子与H、Cl都形成σ键
C.该分子为直线型分子
D.O原子发生sp杂化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将可能含有少量碳、硅杂质的a克镁铝合金投入100 mL一定物质的量浓度的盐酸中,合金部分溶解,过滤,向所得溶液中滴加5 mol/L NaOH溶液至过量,生成沉淀的质量与加入氢氧化钠溶液的体积的关系如图所示。
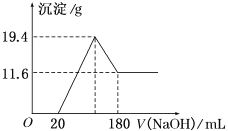
(1)原合金中Mg、Al的质量各是多少?
(2)盐酸的物质的量浓度是多少?
(3)取过滤后所得滤渣,向其中加入足量1mol/L NaOH溶液,可生成标准状况下0.112LH2,则a的最小值是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置,能完成很多电化学实验。下列有关此装置的叙述中,错误的是( )

A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,这种方法称为外加电流的阴极保护法
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处时,铁电极上的电极反应式为:Cu2++2e-===Cu
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处时溶液中各离子浓度都不会发生变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com