
| t2~t3 | t4~t5 | t5~t6 |
| K1 | K2 | K3 |
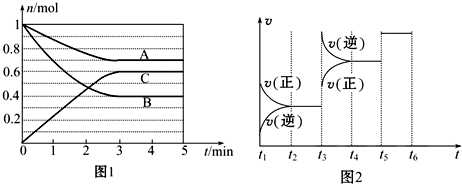
分析 (1)根据图1知,随着反应的进行,A、B的物质的量都减小而C的物质的量增大,则A和B是反应物而Z是生成物,达到平衡状态时△n(A)=(1-0.7)mol=0.3mol、△n(B)=(1-0.4)mol=0.6mol、△n(C)=(0.6-0)mol=0.6mol,同一可逆反应中同一段时间内参加反应的各物质的物质的量之比等于其计量数之比,据此书写方程式;
(2)化学平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比;
(3)①降低温度A的百分含量减小,说明平衡逆向移动,则正反应是吸热反应,该反应的正反应是一个反应前后气体体积减小的吸热反应,在t3时刻改变条件时正逆反应速率都增大,且平衡逆向移动;
②t1~t2时平衡正向移动,t2~t3时反应达到平衡状态,t3~t4时平衡逆向移动;
③该反应的正反应是吸热反应,升高温度化学平衡常数增大,所以温度越高化学平衡常数越大.
解答 解:(1)根据图1知,随着反应的进行,A、B的物质的量都减小而C的物质的量增大,则A和B是反应物而Z是生成物,达到平衡状态时△n(A)=(1-0.7)mol=0.3mol、△n(B)=(1-0.4)mol=0.6mol、△n(C)=(0.6-0)mol=0.6mol,同一可逆反应中同一段时间内参加反应的各物质的物质的量之比等于其计量数之比,A、B、C的计量数之比=0.3mol:0.6mol:0.6mol=1:2:2,所以化学方程式为A+2B?2C,
故答案为:A+2B?2C;
(2)化学平衡常数K=$\frac{{c}^{2}(C)}{c(A).{c}^{2}(B)}$,
故答案为:$\frac{{c}^{2}(C)}{c(A).{c}^{2}(B)}$;
(3)①降低温度A的百分含量减小,说明平衡逆向移动,则正反应是吸热反应,该反应的正反应是一个反应前后气体体积减小的吸热反应,在t3时刻改变条件时正逆反应速率都增大,且平衡逆向移动,改变的条件是升高温度,故答案为:升高温度;
②t1~t2时平衡正向移动,t2~t3时反应达到平衡状态,t3~t4时平衡逆向移动,所以A的转化率最大的是t2~t3,
故答案为:t2~t3;
③t3时刻改变的条件是升高温度,t5改变的条件是加入催化剂,该反应的正反应是吸热反应,升高温度化学平衡常数增大,所以温度越高化学平衡常数越大,所以化学平衡常数大小顺序是K1>K2=K3,
故答案为:K1>K2=K3.
点评 本题考查化学平衡常数计算及外界条件对化学平衡影响,侧重考查学生分析计算能力,化学平衡常数只与温度有关,与物质转化率及物质浓度都无关,题目难度不大.


 高效智能课时作业系列答案
高效智能课时作业系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 托盘两边各垫一张质量相等的纸片称取固体NaOH | |
| B. | 容量瓶内水分未干便注入了液体 | |
| C. | 洗涤刚才盛过溶质的烧杯的洗涤液没有转入容量瓶 | |
| D. | 定容后使溶液混匀,静止,发现凹液面低于刻度线,立即滴加蒸馏水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
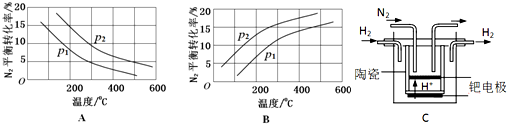
| 反应 | 大气固氮 N2(g)+O2(g)?2NO(g) | 工业固氮 N2(g)+3H2(g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
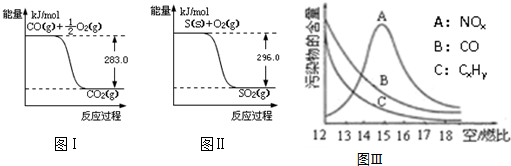
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
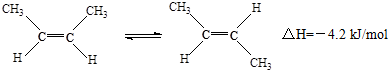
| A. | 顺-2-丁烯比反-2-丁烯稳定 | |
| B. | 顺-2-丁烯的燃烧热比反-2-丁烯大 | |
| C. | 加压和降温有利于平衡向生成顺-2-丁烯反应方向移动 | |
| D. | 它们与氢气加成反应后的产物具有不同的沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2O( mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com