
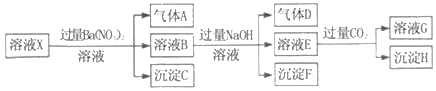
����Ŀ��pH=1��ij��ҺX�н�����NH4+��Al3+��Ba2+��Fe2+��Fe3+��CO32����SO32����SO42����Cl����NO3���е�һ�ֻ��֣�����ˮ�ĵ��뼰���ӵ�ˮ�⣩��ȡ����Һ��������ʵ�飬ʵ�������ͼ�������й��ƶϲ���ȷ���ǣ�������
A. ��ҺX��һ������H+��Al3+��NH4+��Fe2+��SO42��
B. ������������ʵ�鲻��ȷ����ҺX���Ƿ���Fe3+��Cl��
C. ����HΪAl��OH��3��BaCO3�Ļ����
D. ����ҺXΪ100mL������������AΪ44.8mL����״��������X��c��Fe2+��=0.06molL��1
���𰸡�C
��������pH=1����ҺΪǿ������Һ����ǿ������Һ��һ���������CO32����SO32�����ӣ�����������ᱵ���ɳ�������ó���CΪBaSO4��˵����Һ�к���SO42�����ӣ���������A����Aֻ����NO��˵����Һ�к��л�ԭ�����ӣ���һ��ΪFe2+���ӣ���ҺB�м������NaOH��Һ������FֻΪFe��OH��3����������D����DΪNH3��˵����Һ�к���NH4+���ӣ���ҺE��ͨ��CO2���壬���ɳ���H����HΪAl��OH��3��EΪNaOH��NaAlO2��˵����Һ�к���Al3+���ӣ��ٸ������ӹ���֪ʶ����Һ�к���Fe2+���ӣ���һ������NO3-���ӣ�һ������SO42�����ӣ���ô��һ������Ba2+���ӣ�����ȷ���Ƿ��е�����Fe3+��Cl-����A�����ݷ�����֪����Һ��һ�����ڣ�H+��Al3����NH4����Fe2����SO42����A��ȷ��B��������������ʵ�鲻��ȷ����ҺX���Ƿ���Fe3����Cl����B��ȷ��C����������������֪HΪAl��OH��3��BaCO3������Ķ�����̼����̼���Ⱶ��������ˮ��C����D����������A�����ӷ�Ӧ����ʽΪ��3Fe2++NO3-+4H+=3Fe3++NO��+2H2O������������AΪ44.8 mL�����ʵ���Ϊ��0.0448L��22.4L/mol=0.002mol����n��Fe2+��=3��0.002=0.006mol��c��Fe2+��=0.006mol��0.1L=0.06mol/L��D��ȷ����ѡC��


 �п������п��Ծ����ϵ�д�
�п������п��Ծ����ϵ�д� ��������״Ԫ��ϵ�д�
��������״Ԫ��ϵ�д� �ƸԿ�����ҵ��ϵ�д�
�ƸԿ�����ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
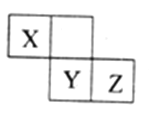
����Ŀ��X��Y��Z���ֶ�����Ԫ�������ڱ��е�λ����ͼ��Xͨ���������Ե����γ�X2���ӣ�����˵������ȷ����
A. ������XZ3�и�ԭ�Ӿ�����8���ӵ��ȶ��ṹ
B. X��Y��Z����Ԫ���γɵĺ����ᶼ��ǿ��
C. �����£�Z���ʿ���Y���⻯����û���Ӧ
D. һ�������£�X2��Al��Ӧ�õ�AlX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽������Na2CO3��NaHCO3���ְ�ɫ��ĩ�����ܴﵽԤ��Ŀ�ĵ���(����)
A. �ֱ�������İ�ɫ��ĩ�мӵ��������Ũ�ȵ�ϡ���ᣬ�Ƚ���������Ŀ���
B. �ֱ�������İ�ɫ��ĩ�мӵ����������ˮ���ȽϹ����ܽ����Ķ���
C. �ֱ����İ�ɫ��ĩ�����Һ��Ȼ��������ʯ��ˮ���Ƚ��Ƿ��г�������
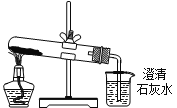
D. �ֱ����İ�ɫ��ĩ����ͼװ�ý���ʵ�飬�Ƚϳ���ʯ��ˮ�Ƿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӻ�������ȡ�ⵥ�ʣ�����Ĺ����������£��ɺ��� ![]() ������
������ ![]() ����Һ
����Һ ![]() ��Һ
��Һ ![]() ��ˮ
��ˮ ![]() I2��CCl4
I2��CCl4
��Һ ![]() I2���й��ں�ˮ�Ƶ��˵����ȷ���ǣ� ��
I2���й��ں�ˮ�Ƶ��˵����ȷ���ǣ� ��
A.ʵ�����������������ոɺ����������ò���������
B.��I������Һ�м���ϡ�����˫��ˮ��Ԫ�ط�����ԭ��Ӧ
C.�ڵ�ˮ�м��뼸�ε�����Һ����Һ������ɫ����
D.��ˮ����CCl4�õ�I2��CCl4��Һ���ò���Ϊ��ȡ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ʵ��С����Ƶ�����ʵ�鲻�������ǣ�������
A. 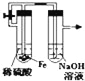 �Ʊ����۲�����������
�Ʊ����۲�����������
B. 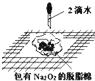 ֤������������ˮ��Ӧ����
֤������������ˮ��Ӧ����
C. 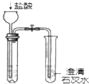 ����̼��������������
����̼��������������
D. 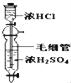 �Ʊ�����������Ȼ�������
�Ʊ�����������Ȼ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
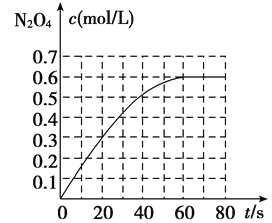
����Ŀ��298 Kʱ����2 L�̶�������ܱ������У��������淴Ӧ��2NO2(g) ![]() N2O4(g)����H����a kJ/mol(a>0)��N2O4�����ʵ���Ũ����ʱ��仯��ͼ����ƽ��ʱ��N2O4��Ũ��ΪNO2��2��������Ӧ��398 K���У�ijʱ�̲��n(NO2)��0.6 mol��n(N2O4)��1.2 mol�����ʱ�����д�С��ϵ��ȷ����(����)
N2O4(g)����H����a kJ/mol(a>0)��N2O4�����ʵ���Ũ����ʱ��仯��ͼ����ƽ��ʱ��N2O4��Ũ��ΪNO2��2��������Ӧ��398 K���У�ijʱ�̲��n(NO2)��0.6 mol��n(N2O4)��1.2 mol�����ʱ�����д�С��ϵ��ȷ����(����)
A. v(��)>v(��)
B. v(��)<v(��)
C. v(��)��v(��)
D. v(��)��v(��)��С��ϵ��ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�У�����ȡ����Ӧ����
A. ��ϩ��������Ȼ�̼��Һ��Ӧ B. ����һ����������������Ӧ
C. �����������ڹ��������·�Ӧ D. �Ҵ���һ��������������ȩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�С������ͼװ����ȡCl2 �� ֤�������������к���HCl�� 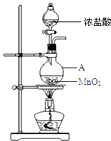
��1������A������Ϊ��A�з�Ӧ�����ӷ���ʽΪ��
��2����ͬѧ��A�в���������ͨ�������Һ��
ʵ����� | �Լ� | ���� |
a | ��ɫʯ����Һ | |
b | AgNO3��Һ | ���ְ�ɫ���� |
��ʵ��a�е�����Ϊ��
�ڲ���֤�������������к���HCl��ʵ����������ĸ��ţ���
��3����֪��HCl����ͨ�뱥��ʳ��ˮ���а�ɫ������������ͬѧ��A�в���������ͨ�뱥��ʳ��ˮ�У��а�ɫ��������������ʵ�鲻��֤�������к���HCl����ϻ�ѧ���������ԭ����
��4����֪��2S2O32��+I2�TS4O62��+2I�� �� ��ͬѧ��A�в���������ͨ������ˮ�У��õ���ҺX����������ʵ��֤�������к���HCl��
I���ⶨX���ܽ��Cl2 �� ȡ25.00mL��ҺX���������KI��Һ��Ȼ����0.04molL��1 Na2S2O3��Һ�ζ�����
��I2 �� ��ζ��յ�ʱ����Na2S2O3��ҺV mL��
�ⶨX��ClԪ����������ȡ25.00mL��ҺX��ѡ���ʵ��Ļ�ԭ�����ܽ��Cl2ȫ����ԭΪCl�� �� ����0.10molL��1 AgNO3��Һ�ζ�������Һ�е�Cl�� ��
��X�е�HClO����Ӱ��I�IJⶨ�����ԭ������
����I������ʵ�����ݿ�֤��A�в����������к���HCl�����������0.10molL��1 AgNO3��Һ�����Ӧ����mL���ú�V�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.ϡ������Ԫ�ػ�ѧ���ʲ����ã�������������Ϊ8
B.���������⣬�������ھ���18��Ԫ��
C.����Ԫ��û�зǽ���Ԫ��
D.�����Ԫ����ָ�ڢ�A�������Ԫ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com