
室温下,现有三种酸,a盐酸、b乙酸、c硫酸的稀溶液,下列说法正确的是( )
|
| A. | 同浓度,pH由大到小:c>a>b |
|
| B. | 同浓度同体积,分别与氢氧化钠中和,所需的氢氧化钠的物质的量由大到小:c>a>b |
|
| C. | 同pH,物质的量浓度由大到小:b>a>c |
|
| D. | 同pH同体积,分别于少量且质量相同的Zn片反应,反应所需时间由长到短:b>a>c |
考点:
弱电解质在水溶液中的电离平衡.
专题:
电离平衡与溶液的pH专题.
分析:
A.同浓度时,氢离子浓度大小顺序是c>a>b,氢离子浓度越大其pH越小;
B.同浓度同体积时,消耗氢氧化钠的物质的量与氢离子的物质的量成正比;
C.同pH时,相同元数的酸,酸的电离程度越大其浓度越小,强酸溶液中,酸的浓度与元数成反比;
D.同pH同体积,分别于少量且质量相同的Zn片反应,反应过程中,氢离子浓度越大其反应速率越大.
解答:
解:A.同浓度时,氢离子浓度大小顺序是c>a>b,氢离子浓度越大其pH越小,则pH大小顺序是b>a>c,故A错误;
B.同浓度同体积时,消耗氢氧化钠的物质的量与氢离子的物质的量成正比,硫酸消耗氢氧化钠最多,醋酸和盐酸物质的量相等且都是一元酸,所以二者消耗NaOH的物质的量相等,则所需的氢氧化钠的物质的量由大到小:c>a=b,故B错误;
C.同pH时,相同元数的酸,酸的电离程度越大其浓度越小,强酸溶液中,酸的浓度与元数成反比,所以pH相等的这三种酸,其物质的量浓度大小关系为b>a>c,故C正确;
D.同pH同体积,分别于少量且质量相同的Zn片反应,反应过程中,氢离子浓度越大其反应速率越大,随着反应的进行,醋酸中氢离子浓度最大,盐酸和硫酸中氢离子浓度相等,所以反应速率大小顺序是b>a=c,反应所需时间由长到短:b<a=c,故D错误;
故选C.
点评:
本题考查了弱电解质的电离,明确弱电解质电离特点是解本题关键,知道溶液pH与其浓度、电解质强弱的关系,注意不同酸与同一金属反应时,反应速率与氢离子浓度有关而与电解质强弱无关,为易错点.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
某溶液可能含有Cl-、SO 、CO
、CO 、NH
、NH 、Fe3+、Fe2+、
、Fe3+、Fe2+、
Al3+和Na+。某同学为了确认其成分,取部分试液,设计并完成了如下实验:
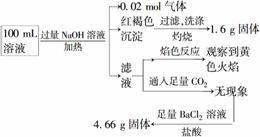
下列说法正确的是( )
A.原溶液中c(Fe3+)=0.2 mol·L-1
B.要确定原溶液中是否含有Fe2+,其操作为取少量原溶液于试管中,加KSCN溶液,再加入适量
氯水,溶液呈血红色,则含有Fe2+
C.SO 、NH
、NH 、Na+一定存在,CO
、Na+一定存在,CO ,Al3+一定不存在
,Al3+一定不存在
D.溶液中至少有4种离子存在,其中Cl-一定存在,且c(Cl-)≥0.2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
关于晶体的下列说法正确的是( )
①在晶体中只要有阴离子就一定有阳离子,只要有阳离子就一定有阴离子;②分子晶体的熔点一定比金属晶体的低;③晶体中分子间作用力越大,分子越稳定;④离子晶体中,一定存在离子键;⑤分子晶体中,一定存在共价键;⑥原子晶体中,一定存在共价键;⑦熔融时化学键没有破坏的晶体一定是分子晶体.
|
| A. | ②④⑥ | B. | ④⑤⑦ | C. | ④⑥⑦ | D. | ③④⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是某太空空间站能量转化系统的局部示意图,基中燃料电池采用KOH为电解液,下列有关说法中正确的是( )
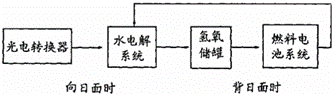
|
| A. | 该能量转化系统工作时,需不断补充H2O |
|
| B. | 该转化系统的能量本质上来源于太阳能 |
|
| C. | 水电解系统中的阴极反应:4OH﹣﹣4e﹣=O2+2H2O |
|
| D. | 燃料电池放电时的负极反应:H2﹣2e﹣=2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,将等物质的量的P与Q投入体积固定2L密闭容器中,发生反应2P(g)+Qg)⇌xW(g)+U(g),经5min后到达平衡,这5min内W的平均反应速率是0.2mol/(L•min),平衡时U的浓度为0.5mol/L,[P]:[Q]=1:2,下列说法中不正确的是( )
|
| A. | x值是2 |
|
| B. | P平衡转化率为66.7% |
|
| C. | 平衡常数为1 |
|
| D. | 反应前,Q的物质的量为3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
火力发电厂在发电过程中会释放大量的
SO2,CO,NO而造成污染,对燃煤烟气进行脱硫、脱碳、脱硝等处理,以实现绿色环保、废物利用的目的.
(1)脱硫.
①用采用活性炭吸附含SO2废气,2SO2+O2⇌2SO3
某研究小组研究燃煤烟气流速、温度、水蒸气含量等因素对SO2吸收效率的影响,实验结果如左图所示.
A 水蒸气含量10%,燃煤烟气流速0.01L/s
B 水蒸气含量5%,燃煤烟气流速0.01L/s
C水蒸气含量5%,燃煤烟气流速0.025L/s
根据左图所示,要提高燃煤烟气中SO2的吸收效率,烟气流速应选择 L/s,温度应选择 (填“高温”或“低温”),应该 水蒸气含量(填“提高”或“降低”)
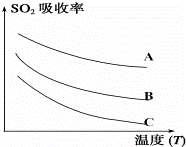
②用惰性电极电解SO2水溶液:H2SO3 O2↑+S↓+H2O
O2↑+S↓+H2O
装置如右图所示,S单质将在 极得到(填“a”或“b”)
该电极的电极反应式
不考虑溶液体积的变化,电解槽右池的pH将
(填“上升”、“降低”或“不变”)
| 物质 | CO | H2O | HCOOH |
| 浓度/mol•L﹣1 | 0.5 | 1.5 | 0.5 |
(2)脱碳.将CO转化为甲酸HCOOH的反应为CO(g)+H2O(g)⇌HCOOH (g),某温度下的平衡常数为1.5.此温度下,密闭容器中加入CO(g)与H2O(g),某时刻测得各组分的浓度如右表:
反应的平衡常数表达式 K= ;比较此时正、逆反应速率的大小:v正 v逆(填“>”、“<”或“=”).到达平衡时H2O的平衡转化率为 .
(3)脱硝.①烟气联合脱硝脱硫,可以有效提高可以显著提高SO2吸收效率,其主要原因在于NO对2SO2+O2⇌2SO3起催化作用,试用化学方程式表示该过程(提示:催化剂参与反应,但是质量和化学性质在反应前后都没有改变) 、 (不必配平)
②可以利用烟气中CO作为还原剂,催化还原NO,同步脱硝脱碳,
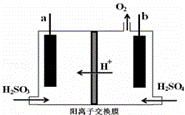
CO(g)+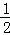 O2(g)=CO2(g)△H=﹣283.0kJ•mol﹣1;N2(g)+O2(g)=2NO(g)△H=182.6kJ•mol﹣1
O2(g)=CO2(g)△H=﹣283.0kJ•mol﹣1;N2(g)+O2(g)=2NO(g)△H=182.6kJ•mol﹣1
NO与CO反应得到无污染产物的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
橡胶属于重要的工业原料.它是一种有机高分子化合物,具有良好的弹性,但强度较差.为了增加某些橡胶制品的强度,加工时往往需进行硫化处理.即将橡胶原料与硫磺在一定条件下反应;橡胶制品硫化程度越高,强度越大,弹性越差.下列橡胶制品中,加工时硫化程度较高的是( )
|
| A. | 橡皮筋 | B. | 汽车外胎 | C. | 普通气球 | D. | 医用乳胶手套 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下表给出了五种元素的相关信息,其中A、B、C、D为短周期元素.
| 元素 | 相关信息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为倍受青睐的清洁燃料. |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障. |
| C | 植物生长三要素之一,它能形成多种氧化物,其中一种是早期医疗中使用的麻醉剂. |
| D | 室温下其单质呈粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰. |
| E | 它是人体不可缺少的微量元素,其单质也是工业生产中不可缺少的金属原材料,常用于制造桥梁、轨道等. |
根据上述信息填空:
(1)B在元素周期表中的位置是
(2)D的单质与烧碱水溶液加热时自身的氧化还原反应生成两种具有强还原性的阴离子,写出该反应的离子方程式 .
(3)C与A形成的化合物X,分子中原子个数比为1:2;相同条件时,相同质量时,氢气的体积为X气体体积的16倍;分子中有极性键和非极性键,可作火箭燃料.写出X分子的结构式
(4)以上这五种元素能组成一种工业上用途极广的复盐(类似明矾,含一种阴离子和两种阳离子),该物质中的A、B、C、D、E的质量比为5:56:7:16:14.请写出该化合物的化学式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com