
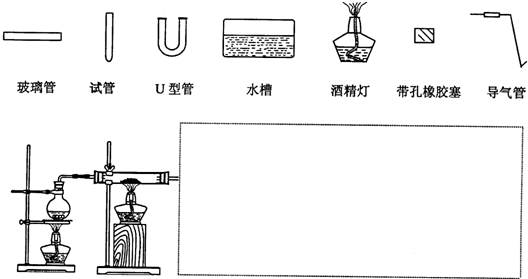
分析 (1)根据现象判断产物为四氧化三铁和氢气;
(2)证明铁和水蒸气反应的方法可以根据固体的性质验证分析,也可以依据生成的气体为氢气;
(3)氢气的密度比空气的小,且不溶于水;
(4)Fe3+使KSCN溶液变红,Fe2+使高锰酸钾酸性溶液褪色;
(5)铁粉将溶液中的Fe3+全部还原为Fe2+;
(6)①氧气能将Fe(OH)2沉淀氧化为氢氧化铁;
②Fe(OH)2沉淀易被氧气氧化,应除掉溶液中的氧气和隔绝空气.
解答 解:(1)铁和水蒸气反应的化学方程式为:3Fe+4H2O(g) $\frac{\underline{\;\;△\;\;}}{\;}$ Fe3O4+4H2↑,故答案为:3Fe+4H2O(g) $\frac{\underline{\;\;△\;\;}}{\;}$ Fe3O4+4H2↑;
(2)证明还原铁粉与水蒸气发生了反应的方法是收集气体进行爆鸣实验,证明铁发生了反应,故答案为:检验是否有H2产生;
(3)氢气的密度比空气的小,且不溶于水,实验装置示意图 ,故答案为:
,故答案为: ;
;
(4)Fe3+使KSCN溶液变红,Fe2+使高锰酸钾酸性溶液褪色,故答案为:各取少量溶液于两试管中,向其中一试管中滴入几滴KSCN溶液,向另一试管中加入高锰酸钾酸性溶液,观察溶液颜色变化,若前者溶液颜色变红,后是溶液紫红色褪去,则说明溶液中既有Fe2+又有Fe3+;
(5)铁粉将溶液中的Fe3+全部还原为Fe2+,即便加KSCN溶液也不变红色,故答案为:如果反应后混合物中的铁粉过量,铁粉将溶液中的Fe3+全部还原为Fe2+,即便加KSCN溶液也不变红色.反应的离子方程式为Fe+2Fe3+=3Fe2+;
(6)①氧气能将Fe(OH)2沉淀氧化为氢氧化铁,化学方程式:4Fe(OH)2+O2+2H2O═4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
②Fe(OH)2沉淀易被氧气氧化,应除掉溶液中的氧气和隔绝空气,故答案为:第一种:用一只容器较大针孔较细的注射器吸取滤液后再吸入NaOH溶液,然后倒置2~3次;
第二种:向滤液中加入植物油,使滤液与空气隔绝,然后再将滴管伸入水溶液中滴加氢氧化钠溶液;
第三种:向热的硫酸亚铁溶液中滴加热的氢氧化钠溶液,减少溶液中氧气的含量.
点评 本题考查铁及其化合物的性质实验,题目难度不大,注意Fe2+与Fe3+的转化.


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 序号 | 反应 温度/℃ | c(HCl)/ mol•L-1 | v(HCl) /mL | 碳酸钙的形状 | t/min |
| 1 | 20 | 2 | 10 | 块状 | t1 |
| 2 | 20 | 2 | 10 | 粉末 | t2 |
| 3 | 20 | 4 | 10 | 粉末 | t3 |
| 4 | 40 | 2 | 10 | 粉末 | t4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加水溶解,用红色石蕊试纸测其溶液的酸碱性 | |
| B. | 加强碱溶液后加热,滴入酚酞试液,观察溶液颜色 | |
| C. | 加热,将湿润的红色石蕊试纸放在管口观察现象 | |
| D. | 加苛性钠溶液后加热,用湿润的红色石蕊试纸放在试管口进行检验 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com