

| n |
| V |


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
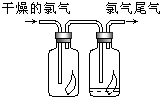 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4、Na2CO3、CaCl2 |
| B、HCl、NaOH、CuSO4 |
| C、H2CO3、CaO、Na2SO4 |
| D、HNO3、Ca(OH)2、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
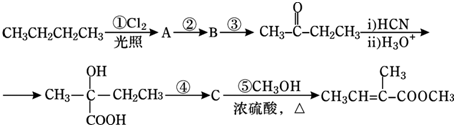
| H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素周期律是指元素的性质随着元素相对原子质量的递增而呈周期性变化的规律 |
| B、改变影响化学平衡的一个因素,平衡将向着抵消这种改变的方向移动 |
| C、酸碱质子理论提出凡是能给出质子的物质都是酸,能接受质子的物质都是碱 |
| D、将NH3通入CO2的NaCl饱和溶液中,可生成溶解度较小的NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中由水电离出的OH一离子浓度c(OH一)=1×10一10?L-1 |
| B、溶液中存在:c(H+)?c(OH一)=l×10-14mol2?L-2 |
| C、溶液中存在:c(Na+)>c(CH3COO一)>c(OH一)>c(H+)>c(CH3COOH) |
| D、溶液中存在:c(CH3COOH)+c(CH3COO一)=c(Na+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com