
| A. | 用澄清石灰水鉴别CO2和SO2 | |
| B. | 用湿润的碘化钾淀粉试纸鉴别Br2(g)和NO2 | |
| C. | 用CO2鉴别Na[Al(OH)4]溶液和NaClO溶液 | |
| D. | 用Ba(OH)2溶液鉴别Na2CO3溶液和NaHCO3溶液 |
分析 A.二者均与石灰水反应生成白色沉淀;
B.二者均能氧化KI;
C.Na[Al(OH)4]溶液与二氧化碳反应生成沉淀,而NaClO不能反应生成沉淀;
D.二者均与氢氧化钡反应生成白色沉淀.
解答 解:A.二者均与石灰水反应生成白色沉淀,现象相同,不能鉴别,故A错误;
B.二者均能氧化KI,试纸均变蓝,不能鉴别,故B错误;
C.Na[Al(OH)4]溶液与二氧化碳反应生成沉淀,而NaClO不能反应生成沉淀,现象不同,可鉴别,故C正确;
D.二者均与氢氧化钡反应生成白色沉淀,现象相同,不能鉴别,故D错误;
故选C.
点评 本题考查物质的鉴别和检验,为高频考点,把握物质的性质、性质差异及反应现象为解答的关键,注意元素化合物知识的综合应用,侧重分析与应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
 我国自主研发制造的国产大型客机C919前不久在上海下线,C919的综合监视电子系统是由无锡企业研发制造.电子监视系统的核心部件是其中的电子芯片.制备该电子芯片的材料是( )
我国自主研发制造的国产大型客机C919前不久在上海下线,C919的综合监视电子系统是由无锡企业研发制造.电子监视系统的核心部件是其中的电子芯片.制备该电子芯片的材料是( )| A. | 铝 | B. | 硅 | C. | 碳 | D. | 钢 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
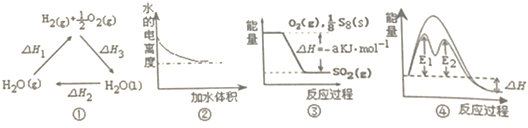
| A. | 图①中△H1=△H2+△H3 | |
| B. | 图②表示0.1mol•L-1氨水加水稀释过程中水的电离度变化曲线 | |
| C. | 图③可知S8燃烧的热化学方程式为S8(s)+8O2(g)=8SO2(g)△H=-8akJ•mol-1 | |
| D. | 图④在催化剂条件下,反应的活化能等于E1+E2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液水电离的c(H+)•c(OH-)=10-24 | B. | c(H+)=10-12mol/L的溶液 | ||
| C. | 甲基橙呈黄色的溶液 | D. | 某溶液与Al粉反应产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0mol•L-1 | B. | 0.1mol•L-1 | C. | 0.3mol•L-1 | D. | 3.0mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
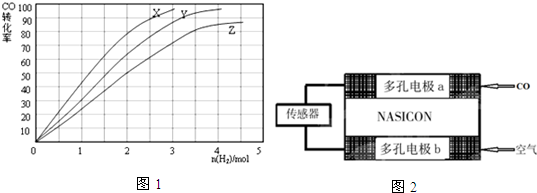
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+ Mg2+ I- SO32- | B. | Mg2+ Na+ CO32- I- | ||
| C. | Al3+Na+ SO32- I- | D. | Na+ CO32- Br-I- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com