
【题目】如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
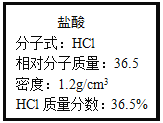
(一)该浓盐酸的物质的量浓度为______mol/L.
(二)某学生欲用上述浓盐酸和蒸馏水配制450mL物质的量浓度为0.3mol/L稀盐酸,可供选用的仪器有:①胶头滴管②烧瓶③烧杯④药匙⑤量筒⑥托盘天平⑦玻璃棒 ,请回答下列问题:
(1)配制稀盐酸时,上述仪器中不需要使用的有______(选填序号),还缺少的仪器有______(写仪器名称).
(2)下列对容量瓶及其使用方法的描述中正确的是______.
A.容量瓶上标有容积、温度和浓度
B.容量瓶用蒸馏水洗净后,必须烘干
C.容量瓶可用来长期储存溶液
D.使用前要检查容量瓶是否漏水
(3)该学生需要量取______mL上述浓盐酸来配制。
(4)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)________________________;
A.用30mL水洗涤烧杯2--3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1-2cm处
(5)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏高”或“偏低”或“无影响”).
I、用量筒量取浓盐酸时俯视观察凹液面______
II、用量筒量取浓盐酸后,洗涤量筒2--3次,洗涤液也转移到容量瓶______
III、溶液注入容量瓶前没有恢复到室温就进行定容______
【答案】12 ②④⑥ 500mL容量瓶 D 12.5 BCAFED 偏低 偏高 偏高
【解析】
(一)利用c=![]() 进行计算;
进行计算;
(二)(1)用盐酸配制溶液,需要用到仪器是量筒、烧杯、胶头滴管、玻璃棒、500mL的容量瓶,据此分析;
(2)根据容量瓶的构造和使用进行分析;
(3)利用稀释前后溶质的物质的量不变进行分析;
(4)配制一定物质的量浓度的溶液的步骤是计算、量取、溶解/稀释、冷却、移液、洗涤、振荡、定容、摇匀、装瓶进行分析;
(5)根据c=![]() 进行分析。
进行分析。
(一)根据c=![]() =
=![]() mol·L-1=12mol·L-1,
mol·L-1=12mol·L-1,
答案:12mol·L-1;
(二)(1) 配制450mL溶液,实验室中没有450mL容量瓶,应选用大而近的容量瓶,即500mL容量瓶,用盐酸配制溶液,需要用到仪器是量筒、烧杯、胶头滴管、玻璃棒、500mL的容量瓶,不需要使用的是②④⑥;缺少的仪器是500mL容量瓶,
答案:②④⑥;500mL容量瓶;
(2)A. 容量瓶上标有容积、使用温度、刻度,没有标明浓度,故A错误;
B. 容量瓶洗涤后是否烘干对实验结果无影响,故B错误;
C. 容量瓶是用来配制一定物质的量浓度溶液的仪器,不能用作稀释、溶解,长期储存溶液的体积,故C错误;
D. 容量瓶使用前需要检查是否漏水,故D正确;
D正确,答案:D;
(3)利用稀释前后溶质的物质的量不变,500×10-3L×0.3mol·L-1=V(HCl)×10-3L×12mol/l,,解得V(HCl)=12.5mL,
答案:12.5;
(4) 配制一定物质的量浓度的溶液的步骤是计算、量取、溶解/稀释、冷却、移液、洗涤、振荡、定容、摇匀、装瓶,顺序是BCAFED,
答案:BCAFED;
(5) 根据c=![]() 进行分析
进行分析
I.用量筒量取浓盐酸时俯视观察凹液面,容量瓶中溶质的物质的量减小,即所配溶液浓度偏低,
答案:偏低;
II.量筒量取浓盐酸后,洗涤量筒将洗涤液转移到容量瓶,造成溶质的物质的量增加,即所配溶液浓度偏高,
答案:偏高;
III.注入容量瓶前没有恢复到室温状态下即定容,利用“热胀冷缩”原理,容量瓶中溶液的体积减小,即所配溶液溶度偏高,
答案:偏高。


科目:高中化学 来源: 题型:
【题目】在FeCl3和CuCl2的混合液中逐渐加入铁粉,溶液中Fe2+的物质的量浓度和加入铁粉的物质的量之间关系如图所示。则该溶液中FeCl3与CuCl2的物质的量浓度之比为

A. 3∶1 B. 1∶2 C. 2∶1 D. 1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO4具有强氧化性,可用作炸药等。实验室由KClO3分解制备KClO4的流程如图:

已知KClO3熔融易烧结,400℃以上分解放出氧气,各物质溶解度如下图。下列说法不正确的是
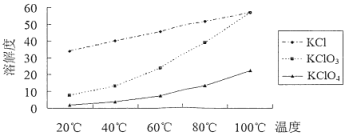
A.实验室制备KClO4的原理为![]()
B.趁热过滤的目的是除去KCl
C.操作①是冷却结晶、过滤、洗涤,操作②是重结晶
D.加热分解时,如果温度过高会使产率下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所给信息或标志,判断下列说法错误的是()
A.在实验室和生产生活中,安全都是避免伤害和事故的保障—用肥皂液涂在天然气管道接口处检验是否漏气
B. 在运送硫酸的油罐车上贴有该标志
在运送硫酸的油罐车上贴有该标志
C. 看到有该标志的丢弃物,应远离并报警
看到有该标志的丢弃物,应远离并报警
D. 贴有该标志的物品是可回收物
贴有该标志的物品是可回收物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知烃D在标准状况下的密度为1.25g·L-1,C、H都是具有浓郁香味、不易溶于水的油状液体。相关物质转化关系如下(转化条件都已省略):
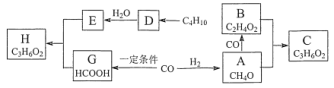
请回答:
(1)B中官能团的名称是____。
(2)C4H10→D的反应条件是____。
(3)E+G→F的化学方程式____。
(4)下列说法正确的是____。
A. C、H属于同一种物质
B. 可以用新制氢氧化铜悬浊液鉴别B、E和G
C. 有机物A、G在一定条件下反应所得产物是B的同分异构体
D. 一定条件下A转化成G,B转化成E,都属于氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E、F均为周期表中前四周期的元素,原子序数依次增大。其中A原子核外有三个未成对电子;化合物B2E为离子晶体,E原子核外的M层中有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体可做半导体材料;F原子最外层电子数与B的相同,其余各层均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)A、B、C、D的第一电离能由小到大的顺序为________
(2)B的氯化物的熔点比D的氯化物的熔点高的理由是____________。
(3)A的简单氢化物的中心原子采取______杂化,E的低价氧化物分子的空间构型是____。
(4)F的核外电子排布式是_____,A、F形成某种化合物的晶胞结构如图所示(其中A显-3价),则其化学式为_______。
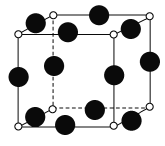
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型锂-空气电池其工作原理如图所示。放电时,O2与Li+在多孔碳材料电极处生成Li2O2-x(x=0或1)。下列说法正确的是
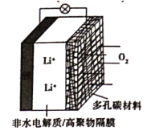
A.锂电极为正极
B.外电路电子由多孔碳材料电极流向锂电极
C.多孔碳材料的O2失电子转化为O2-
D.电池总反应为2Li+(1-x/2)O2=Li2O2-x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将24.4 g NaOH固体溶于水配成100 mL溶液,其密度为1.219 g·mL-1。
(1)该溶液中NaOH的物质的量浓度为________。
(2)该溶液中NaOH的质量分数为________。
(3)从该溶液中取出10 mL,含NaOH的质量为________,含NaOH的物质的量为________。
(4)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A. 用FeCl3溶液腐蚀铜线路板:Cu + Fe3+ = Cu2+ + Fe2+
B. 向氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O = AlO2- + 4NH4+ + 2H2O
C. Na2O2固体与H2O反应产生O2 :2Na2O2 + 2H2O = 4Na+ + 4OH- + O2↑
D. 向酸性KMnO4溶液中通入SO2:3SO2+2MnO+4OH-== 2MnO2↓+3SO![]() +2H2O
+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com