
| A. | CH3-CH2-Br | B. | 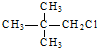 | ||
| C. | 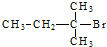 | D. | 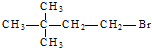 |
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源: 题型:选择题
| A. | 使多糖水解 | B. | 使油脂水解 | C. | 使氨基酸变性 | D. | 使蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
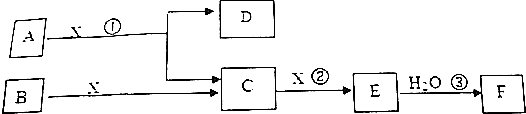
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
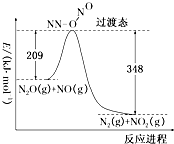
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和甲苯都能与溴水、H2反应 | |
| B. | 聚乙烯的结构简式为CH2=CH2 | |
| C. | 甲苯既能使溴的水溶液褪色,又能在光照下与溴蒸气发生取代反应 | |
| D. | 可用酸性高锰酸钾溶液鉴别乙烯和甲烷或除去甲烷中的乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K2FeO4具有强氧化性,可用作水处理剂 | |
| B. | 氢氧化铝具有弱碱性,可用作制胃酸中和剂 | |
| C. | 碳具有还原性,可用作锌锰干电池的正极材料 | |
| D. | 常温下浓硫酸能使铝发生钝化,可用铝制容器贮运浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com