
【题目】(1)在无土栽培中,配制1 L内含0.5 mol NH4Cl、0.16 mol KCl、0.24 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需这三种固体的物质的量为______、______、________
(2)在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22∶9,当1.6gX与Y完全反应后,生成4.4gR,则此反应中Y和M的质量之比为_________。
(3)一种不纯的铁,已知它含有铜、铝、镁等一种或几种金属杂质,5.6g这样的铁跟足量的稀H2SO4作用,生成H2 2.24L(标准状况),则此铁块中一定含有的金属杂质是____ 。
【答案】0.64mol 0.02mol 0.24mol 16:9 Cu
【解析】
(1)从溶液中离子守恒的物质的量守恒的角度进行计算,依据溶液中各离子的物质的量相等配制。
(2)根据化学方程式和已知条件“R和M的相对分子质量之比为22:9”以及R的质量,列出比例式,即可求出M的质量;根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和。则生成的Y的质量=R的质量+M的质量﹣X的质量,然后写出两者的比即可。
(3)如果Fe是纯铁,根据转移电子守恒知,5.6gFe与足量稀硫酸反应生成n(H2)=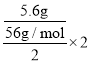 =0.1mol,生成氢气在标况下体积=0.1mol×22.4L/mol,则杂质中金属平均相对原子质量为56,且有能和酸反应生成氢气的、也有和酸不反应的,据此分析解答。
=0.1mol,生成氢气在标况下体积=0.1mol×22.4L/mol,则杂质中金属平均相对原子质量为56,且有能和酸反应生成氢气的、也有和酸不反应的,据此分析解答。
(1)0.5mol NH4Cl、0.16mol KCl、0.24mol K2SO4中 n(NH4+)=n(NH4Cl)=0.5mol;n( Cl﹣ )=n(NH4Cl)+n( KCl)=0.5mol+0.16mol=0.66mol;n( K+ )=n( KCl)+2n( K2SO4)=0.16mol+2×0.24mol=0.64mol;n(SO42﹣)=n( K2SO4)=0.24mol;用KCl、NH4Cl、(NH4)2SO4配制,则:
n((NH4)2SO4)=n(SO42﹣)=0.24mol;
n( KCl)=n( K+ )=0.64mol;
n(NH4Cl)=n( Cl﹣ )﹣n( KCl)=0.66mol﹣0.64mol=0.02mol;
(2)根据已知条件“R和M的相对分子质量之比为22:9”,则R:2M=22:(2×9)=22:18,设生成的M的质量为a,则22:18=4.4g:a,解之得:a=3.6g;
根据质量守恒定律可得Y的质量=4.4g+3.6g﹣1.6g=6.4g;此反应中Y和M的质量比是6.4g:3.6g=16:9。
(3)如果Fe是纯铁,根据转移电子守恒知,5.6gFe与足量稀硫酸反应生成n(H2)=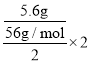 =0.1mol,生成氢气在标况下体积=0.1mol×22.4L/mol,则杂质中金属平均相对原子质量为56(把金属转化为+2价),镁的相对原子质量为24,铝的相对原子质量为27÷3×2=18,都小于56,所以一定含有Cu。
=0.1mol,生成氢气在标况下体积=0.1mol×22.4L/mol,则杂质中金属平均相对原子质量为56(把金属转化为+2价),镁的相对原子质量为24,铝的相对原子质量为27÷3×2=18,都小于56,所以一定含有Cu。


科目:高中化学 来源: 题型:
【题目】SF6是一种无色气体,具有很强的稳定性,可用于灭火,SF6的分子结构如图所示,呈正八面体型。如果F元素有两种稳定的同位素,则SF6的不同分子种数为 ( )

A. 6种B. 7种
C. 10种D. 12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组设计了如图所示的数字化实验装置,研究常温下,向30 mL 0.1 mol·L1 H2A溶液中逐滴加入等浓度NaOH溶液时pH变化情况,并绘制出溶液中含A元素的微粒的物质的量分数与溶液pH的关系(如图所示),下列说法错误的是
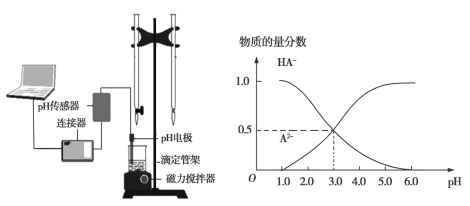
A. pH=4.0时,溶液中n(HA)约为2.73×104 mol
B. 该实验应将左边的酸式滴定管换成右边碱式滴定管
C. 常温下,等物质的量浓度的NaHA与Na2A溶液等体积混合后溶液pH=3.0
D. 0.1 mol·L1NaHA溶液中存在c(A2)+c(HA)+c(H2A)=0.1 mol·L1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把2.7 g铝投入100 mL 3 mol·L-1的NaOH溶液中充分反应后,再滴入1 mol·L-1的盐酸溶液400 mL,其结果错误的是
A. 溶液显酸性B. 得到澄清透明溶液
C. 得到浑浊溶液D. 溶液中铝元素有两种微粒存在形式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求作答:
(1)分子式为C4H8且属于烯烃的有机物的同分异构体(考虑顺反异构)有 _________种;![]() 高聚物的单体的结构简式是_____________ 和______________。
高聚物的单体的结构简式是_____________ 和______________。
(2) ![]() 的名称为:_______________;写出
的名称为:_______________;写出![]() 聚合生成高分子化合物的化学方程式________;
聚合生成高分子化合物的化学方程式________;
(3)已知-NH2表现碱性,-NO2表现中性,-COOH表现酸性。化学式为C7H7NO2的有机物,其分子结构中有1个苯环、2个取代基,试按照下列写出2种同分异构体(只写邻位即可)。
①该有机物既有酸性又有碱性______________。
②该有机物既无酸性又无碱性______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。向A中通入氯气至过量,观察A中,发现溶液先呈红色,然后变为黄色。

(1)A中铁元素发生反应的离子方程式有______________________________________________________。
(2)为了探究A中溶液由红色变为黄色的原因,甲同学进行如下实验:取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在______(填化学符号)。
(3)资料显示:SCN--的电子式为 ![]() 。甲同学猜想SCN― 可能被Cl2氧化了,他进行了如下研究:取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液, 产生白色沉淀,由此证明SCN― 中被氧化的元素是___________(填名称)。
。甲同学猜想SCN― 可能被Cl2氧化了,他进行了如下研究:取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液, 产生白色沉淀,由此证明SCN― 中被氧化的元素是___________(填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为21.则下列说法不正确的是
X | Y | ||
W | Z |
A.原子半径大小:![]()
B.W、Z的最高价氧化物的水化物的酸性,Z强于W
C.可用W与X的氧化物反应来制备X
D.Y与氢元素可以形成原子个数比为1:1的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(H2C2O4)是一种重要的有机化工原料。为探究草酸的制取和草酸的性质,进行如下实验。
实验Ⅰ:探究草酸的制备
实验室用硝酸氧化淀粉水解液法制备草酸:C6H12O6+12HNO3 → 3H2C2O4+9NO2↑+3NO↑+9H2O。装置如下图所示:
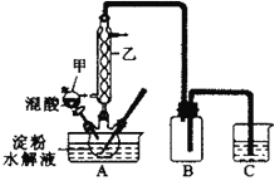
(1)上图实验装置中仪器乙的名称为:___________,B装置的作用____________。
(2)检验淀粉是否完全水解所需要的试剂为:__________。
实验Ⅱ:探究草酸的不稳定性
已知:草酸晶体(H2C2O4·2H2O)无色,易溶于水,熔点为101℃,受热易脱水、升华,170℃以上分解产生H2O、CO和CO2。草酸的酸性比碳酸强,其钙盐难溶于水。
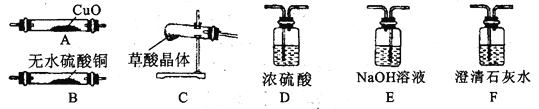
(3)请选取以上的装置证明草酸晶体分解的产物(可重复使用,加热装置和连接装置已略去)。仪器装置连接顺序为:C→______→______→______→______→D→A→F______
(4)若实验结束后测得A管质量减轻4.8g,则至少需分解草酸晶体的质量为_____g(已知草酸晶体的M=126g/mol)。
实验Ⅲ:探究草酸与酸性高锰酸钾的反应
(5)取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色。(反应热效应不明显,可忽略不计)
该实验中草酸表现______性,该反应的离子方程式_____________________________________________,该反应的反应速率先慢后快的主要原因可能是___________________。
(6)设计实验证明草酸是弱酸。实验方案:________________________________ (提供的药品及仪器:蒸馏水、0.1mol·L-1NaOH溶液、pH计、0.1mol·L-1草酸溶液,其它仪器自选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可由乙苯生产苯乙烯:![]() ,下列有关说法正确的是
,下列有关说法正确的是
A. 乙苯和苯乙烯均能发生取代反应、加聚反应和氧化反应
B. 用溴水可以区分苯乙烯和乙苯
C. 1 mol苯乙烯最多可与4 mol氢气加成,加成产物的一氯代物共有5种
D. 乙苯和苯乙烯分子中共平面的碳原子数最多都为7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com