
| A.ΔH1>ΔH2>ΔH3 | B.ΔH1<ΔH2<ΔH3 | C.ΔH1=ΔH2<ΔH3 | D.ΔH1<ΔH2=ΔH3 |
科目:高中化学 来源:不详 题型:单选题
| A.pH=7 | B.C(A-)>c(B+) |
C.C(OH-)=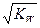 | D.C(H+)- C(OH-)=C (A-)- C(B+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2XY3(g) △H=-92.6 kJ·mol-1
2XY3(g) △H=-92.6 kJ·mol-1| 容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放热 23.15 kJ |
| ② | 0.6 | 1.8 | 0.8 | Q(Q>0) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠与乙醇反应,钠块沉在乙醇液面下面 |
| B.除去乙酸乙酯中残留的乙酸,可用饱和Na2CO3溶液洗涤后分液 |
| C.伴有能量变化的物质变化都是化学变化 |
| D.化学反应达到平衡状态时,只要条件不改变,各物质的浓度就不再改变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 共价键 | H-H | O=O | H-O |
| 键能/kJ ·mol-1 | 436 | 498 | X |
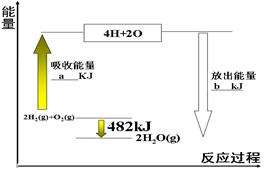
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的___①__产生 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是_ ② 反应 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有_③___生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Sn(白,s)ΔH3=+2.1 kJ·mol-1
Sn(白,s)ΔH3=+2.1 kJ·mol-1| A.ΔH1>ΔH2 |
| B.锡在常温下以灰锡状态存在 |
| C.灰锡转化为白锡的反应是放热反应 |
| D.锡制器皿长期处在低于13.2 ℃的环境中,会自行毁坏 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com