
| A. | 钠在空气中易被氧化,需将其保存在酒精中 | |
| B. | 能使润湿的红色石蕊试纸变成蓝色的气体一定是NH3 | |
| C. | 向某有色溶液中通入SO2气体,溶液变为无色,证明SO2具有漂白性 | |
| D. | 向某溶液中加入BaCl2溶液,产生能溶于稀盐酸的白色沉淀,该溶液一定含有CO32- |
分析 A.钠与乙醇反应;
B.能使润湿的红色石蕊试纸变成蓝色,该气体为碱性气体;
C.二氧化硫能够使高锰酸钾褪色,体现还原性;
D.亚硫酸根离子与钡离子生成的亚硫酸钡也能溶于盐酸.
解答 解:A.钠与乙醇反应,不能保存在乙醇中,故A错误;
B.氨气是碱性其气体,能够能使润湿的红色石蕊试纸变成蓝色,故B正确;
C.二氧化硫能够使高锰酸钾褪色,体现还原性,不体现漂白性,故C错误;
D.向某溶液中加入BaCl2溶液,产生能溶于稀盐酸的白色沉淀,该溶液可能含有碳酸根离子或者亚硫酸根离子,故D错误;
故选:B.
点评 本题考查了元素化合物知识,熟悉钠、二氧化硫、氨气的性质是解题关键,注意离子检验应排除杂质离子的干扰


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
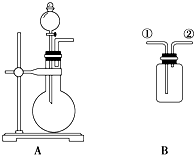 如图A是实验室制取某些气体的装置.
如图A是实验室制取某些气体的装置.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
一定条件下,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用食醋除去水瓶中的水垢:CO32-+2CH3COOH═2CH3COO-+CO2↑+H2O | |
| B. | 用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| C. | 用稀氢氧化钠溶液吸收二氧化氮:2OH-+2NO2═NO3-+NO↑+H2O | |
| D. | 等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应:Ba2++2OH-+2NH4++SO42-═BaSO4↓+2NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 HCO3-+OH-,与油污发生反应,达到去污目的.
HCO3-+OH-,与油污发生反应,达到去污目的.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
 (填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式
(填该物质的电子式)③加成反应(填反应类型)写出第一步的化学方程式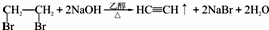 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
| 建筑垃圾 | 二氧化碳 | 氟利昂 | 二氧化硫 |
| 白色污染 | 温室效应 | 臭氧层受损 | 酸雨 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com