
【题目】FeCl3在现代工业生产中应用广泛。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。工业上,向500—600℃的铁屑中通入氯气可生产无水氯化铁;向炽热铁屑中通入氯化氢可以生产无水氯化亚铁。
某化学研究性学习小组模拟工业生产流程制备无水FeCl3并对产物做了如下探究实验,请回答下列问题:
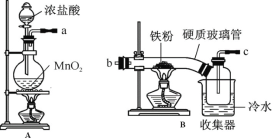
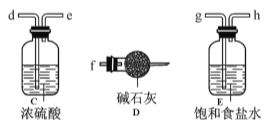
(1)装置的连接顺序为 (用a 、b、c…h表示)。
(2)i.A装置中反应的化学方程式为 。
ii.D中碱石灰的作用是 。
(3)反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端。要使沉积得FeCl3进入收集器,需进行的操作是 。
(4)FeCl3溶液常用于吸收有毒气体H2S。反应的离子方程式为 。
(5)反应一段时间后熄灭酒精灯,冷却后将硬质玻璃管及收集器中的物质一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(过程中不振荡),充分反应后,进行如下实验:

淡黄色溶液中加入试剂X生成淡红色溶液的离子方程式为 。
(6)已知红色褪去的同时有气体生成,经检验为O2。该小组同学对红色褪去的原因进行探究。
①取褪色后溶液三份,第一份滴加FeCl3溶液无明显变化;第二份滴加试剂X,溶液出现红色;第三份滴加稀盐酸和BaCl2溶液,产生白色沉淀。
②另取同物质的量浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化。
根据上述实验得出溶液褪色的原因是: 。
【答案】
(1)aghdebcf;
(2)i.MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;ii.吸收没有反应完的氯气,以防污染空气;
MnCl2+Cl2↑+2H2O;ii.吸收没有反应完的氯气,以防污染空气;
(3)在沉积的FeCl3固体下方加热;
(4)2Fe3++2H2S=2Fe2++2H++S↓;
(5)Fe3++3SCN-![]() Fe(SCN)3;
Fe(SCN)3;
(6)H2O2将SCN-氧化成SO42—;
【解析】
试题分析:(1)浓硫酸具有吸水性能作氯气干燥剂、碱石灰具有碱性而吸收氯气、饱和食盐水吸收氯化氢而抑制氯气溶解,装置排列顺序为气体的制取→洗气→干燥→氯气和铁的反应→尾气处理,所以装置连接顺序为a→g→h→d→e→b→c→f,故答案为:a、g、h、d、e、b、c、f;
(2)i.A装置中二氧化锰与浓盐酸反应生成氯气,反应的化学方程式为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
ii.D中碱石灰的作用是吸收多余污染气体,防止空气中水蒸气进入装置B,吸收没有反应完的氯气,以防污染空气, 故答案为:吸收没有反应完的氯气,以防污染空气;
(3)无水FeCl3在空气中易潮解,加热易升华,反应结束后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管B中硬质玻璃管的右端.要使沉积得FeCl3进入收集器,需进行的操作是在沉积的FeCl3固体下方加热,故答案为:在沉积的FeCl3固体下方加热;
(4)Fe2+被H2O2氧化生成Fe3+,从而增大Fe3+浓度,Fe3+、SCN-反应生成Fe(SCN)3,从而增大络合物浓度,溶液颜色加深,反应的化学方程式为:2Fe2++2H++H2O2═2Fe3++2H2O,故答案为:2Fe2++2H++H2O2═2Fe3++2H2O;
(5)Fe3+和KSCN反应生成络合物硫氰化铁而使溶液呈血红色,反应方程式为Fe3++3SCN-![]() Fe(SCN)3,故答案为:Fe3++3SCN-
Fe(SCN)3,故答案为:Fe3++3SCN-![]() Fe(SCN)3;
Fe(SCN)3;
(6)根据①滴加FeCl3溶液无明显变化,说明SCN-发生了反应而不是Fe3+发生反应,滴加稀HCl和BaCl2溶液,产生白色沉淀,说明生成了硫酸根;根据②另取同浓度的 FeCl3溶液滴加2滴试剂X,溶液变红,再通入O2,无明显变化,说明O2不能氧化SCN-,所以氧化SCN-的为双氧水;故答案为:H2O2将SCN-氧化成SO42-。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】随着卤族元素原子序数递增,下列说法正确的是( )
A.单质的氧化性逐渐减弱
B.单质的熔、沸点逐渐降低
C.单质的密度逐渐降低
D.气态氢化物的稳定性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将2molA和3molB充入一密闭的容器中发生反应:aA(g)+B(g)![]() C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则
C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则
A. a="3" B. a="2" C. B的转化率为40% D. B的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度为c mol/L,体积为V mL的AgNO3溶液分别与100 mL NaCl、MgCl2、AlCl3溶液恰好完全反应,则这三种溶液的物质的量浓度之比为
A.6∶3∶2 B.1∶2∶3 C.2∶3∶6 D.2∶6∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①液态HCl ②NaHCO3 ③NaCl溶液 ④CO2 ⑤蔗糖晶体 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁胶体 ⑧NH3·H2O ⑨空气 ⑩Al2(SO4)3
(1)上述十种物质中有两种物质在水溶液中可发生反应,离子方程式为:H++OH-===H2O,该反应的化学方程式为_____________________。
(2)⑩在水中的电离方程式为___________________________。
(3)胃液中含有盐酸,胃酸过多的人常有胃疼烧心的感觉,易吐酸水,服用适量的小苏打(NaHCO3),能
治疗胃酸过多,请写出其反应的离子方程式:________________________;如果病人同时患胃溃疡,为防胃壁穿孔,不能服用小苏打,此时最好用含Al(OH)3的胃药(如胃舒平),它与胃酸反应的离子方程式:________________________。
(4)写出下列反应的离子方程式
向Ba(OH)2溶液中逐滴加入稀硫酸________________________。
向Ba(OH)2溶液中通入过量的CO2_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱性锌锰干电池的总反应方程式可以表示为:Zn+2MnO2+2H2O==Zn(OH)2+2MnOOH 此电池放电时,正极上发生反应的物质是( )
A. 碳棒 B. MnO2和H2O C. Zn D. MnO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关方程式书写正确的是
A.FeCl2溶液中加入氯水的离子方程式:Fe2++ Cl2=Fe3++2Cl-
B.食醋与NaOH反应的离子方程式:H++OH-=H2O
C.CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
D.Na2O2与水反应的离子方程式:2O22-+ 2H2O = 4OH-+ O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com