
【题目】海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。
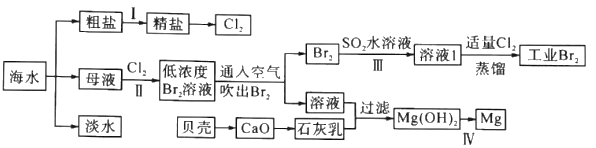
请回答下列问题:
(1)步骤I中,粗盐中含有Ca2+、Mg2+、SO42-等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是______(填字母)。
A.①②③④ B.②③④① C.②④③① D.③④②①
请写出加入Na2CO3溶液后相关化学反应的离子方程式:_________、_________。
(2)步骤Ⅱ中已获得Br2,步骤Ⅲ中又将Br2还原为Br-,其目的是_________。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为_________。
(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2.可向其中加入_________溶液。
(4)步骤Ⅳ由Mg(OH)2得到单质Mg,以下方法最合适的是_________(填序号)。
A. ![]()
B.![]()
C.![]()
D. ![]()
【答案】 B、C Ca2++CO32-==CaCO3↓ Ba2++ CO32-==BaCO3↓ 富集(或浓缩)溴元素 Br2+SO2+2H2O=4H++2Br-+SO42- NaBr(或溴化钠) C
【解析】(1)除去粗盐中的Ca2+、Mg2+、SO42-,盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,要先加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除过量的钡离子;(2)海水中溴的浓度太低,要进行富集。(3)利用氯的氧化性强于溴,Cl2+2Br-=2Cl-+Br2;(4)海水中加入试剂氢氧化钙沉淀镁离子生成氢氧化镁沉淀,过滤后在氢氧化镁沉淀中加入试剂盐酸溶解,得到氯化镁溶液,通过操作浓缩蒸发,冷却结晶得到氯化镁晶体,在氯化氢气流中加热失水得到无水氯化镁,电解熔融氯化镁得到金属镁;
(1)要先除硫酸根离子,然后再除钙离子,碳酸钠可以除去过量的钡离子,如果加反了,过量的钡离子就没法除去,至于加氢氧化钠除去镁离子顺序不受限制,因为过量的氢氧化钠加盐酸就可以调节了,只要将三种离子除完了,过滤就行了,最后加盐酸除去过量的氢氧根离子碳酸根离子,顺序为: B.②③④①或 C.②④③① ,故选BC。(2)步骤Ⅱ中已获得Br2,但浓度太稀,步骤Ⅲ中又将Br2还原为Br-,其目的是富集(或浓缩)溴元素 。步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,SO2将溴还原为Br-,有关反应的离子方程式为 Br2+SO2+2H2O=4H++2Br-+SO42-。(3)为了从工业Br2中提纯溴,除去产物中残留的少量Cl2.利用氯的氧化性强于溴,可向其中加入NaBr(或溴化钠)溶液,Cl2+2Br-=2Cl-+Br2。(4)海水中加入试剂氢氧化钙沉淀镁离子生成氢氧化镁沉淀,过滤后在氢氧化镁沉淀中加入试剂盐酸溶解,得到氯化镁溶液,通过操作浓缩蒸发,冷却结晶得到氯化镁晶体,在氯化氢气流中加热失水得到无水氯化镁,电解熔融氯化镁得到金属镁;步骤Ⅳ由Mg(OH)2得到单质Mg,最合适的方法是C。A、氧化镁熔点太高,故A错误;B、MgO离子化合物,很稳定,高温也不分解,故B错误;D、电解MgCl2水溶液只能得到氢氧化镁、氢气和氯气,故D错误;故选C。


 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:
【题目】不能用离子方程式CO32﹣+2H+→CO2↑+H2O表示的是( )
A.Na2CO3+2HCl→2NaCl+CO2↑+H2O
B.NaHCO3+HCl→NaCl+CO2↑+H2O
C.K2CO3+H2SO4→K2SO4+CO2↑+H2O
D.K2CO3+2HNO3→2KNO3+CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列叙述正确的是
A. 标准状况下,1.12 L CCl4含有质子数的数目为3.7NA
B. 常温常压下,3.0 g含葡萄糖的冰醋酸中含有的原子总数为0.4NA
C. 常温时,56g Fe与足量浓硝酸反应,转移的电子数目为3NA
D. 晶体B的结构单元如右图 ,则11g晶体B含有0.6NA个三角形(相邻原子构成)
,则11g晶体B含有0.6NA个三角形(相邻原子构成)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物的结构简式中,书写正确的是( )
A. CH2CH2 B. C2H5OOCCH3 C. CH3—CH—CH3 D. CH3C—OOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C,D、E、G六种前四周期主族元素,已知A、B、C、D、E五种元素在元素周期表中的位置如图所示。

(1)若非金属元素B的核电荷数为x,则A、B、C、D、E五种元素的核电荷数之和为_________。
(2)若A、B、C、D四种元素的核内质子数之和为56,lmolG的单质与足量盐酸反应,能产生22. 4LH2(在标准状况下);G的阳离子与D的阴离子核外电子层结构相同。
①写出下列元素名称:A_________,B________;
②D的简单离子结构示意图为_________;
③氢化物的沸点:D_________B,简单氢化物水溶液的酸性:B_________C(填“>”“<”或“=”)。
④甲为G、C两元素组成的化合物,用电子式表示甲的形成过程_________。
(3)下列说法正确的是_________(填序号)
A.氢键是极弱的化学键,任何物质中都存在化学键
B.共价化合物中成键原子均满足稀有气体的稳定结构
C.两种非金属元素形成的化合物可能含有离子键
D.化学键断裂,一定发生化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对炼锌厂的铜镉废渣中各元素进行分离,能减少环境污染,同时制得食品锌强化剂的原料ZnSO4·7H2O实现资源的再利用。其流程图如下。

[相关资料]
①铜镉废渣中含有铜、锌、镉、铁、砷等元素,其含量依次减少。
②FeAsO4难溶于水;ZnSO4·7H2O易溶于水,难溶于酒精。
③Zn(OH)2属于两性氢氧化物。
④滤液I中有Fe2+、Zn2+、Cu2+、Cd2+和少量的AsO![]() 。
。
⑤有关离子沉淀完全的pH
金属离子 | Fe3+ | Zn2+ | Mn2+ | Cu2+ | Cd2+ |
沉淀完全pH | 3.2 | 8.0 | 9.8 | 6.4 | 9.4 |
请回答下列问题:
(1)提高铜镉废渣浸出率可以采用的方法是(写出其中一点即可)____;
(2)向滤液I中逐滴滴人酸性KMnO4溶液可与AsO![]() 发生反应生成FeAsO4,写出该反应的离子方程式____;加入酸性KMnO4溶液不能过量,判断该滴定终点的现象是____;滤渣Ⅱ中除了FeAsO4外,还有____;
发生反应生成FeAsO4,写出该反应的离子方程式____;加入酸性KMnO4溶液不能过量,判断该滴定终点的现象是____;滤渣Ⅱ中除了FeAsO4外,还有____;
(3)制得的ZnSO4·7H2O需洗涤,洗涤晶体时应选用试剂为____;
(4)上述流程除了实现对这些元素进行提取分离能减少环境污染,同时制得ZnSO4·7H2O实现资源的再利用,还可以得到副产物___
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池的工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的正极反应式为____;
(6)若a克铜镉废渣含有b molFe元素,加入了c mol KMnO4,则铜镉废渣中As元素的质量分数为____。(不考虑镉元素与KMnO4的反应)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)25℃时,在0.1L 0.2molL﹣1的HA溶液中,有0.001mol的HA电离成离子,则该溶液的pH= .
(2)25℃时,若向0.1mol/L氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=amol/L,则c(SO42﹣)= .
(3)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是 .
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
化学式 | 电离常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×l0﹣7、K2=5.6×10﹣11 |
回答下列问题
25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为 .
向NaCN溶液中通入少量CO2 , 所发生反应的化学方程式为: .
(5)常温下,在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液的体积之和,则Ba(OH)2溶液与NaHSO4溶液的体积比是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为2Cu+Ag2O==Cu2O+2Ag,下列有关说法正确的是( )
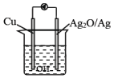
A. 测量原理示意图中,电子方向从Ag2O→Cu
B. 反应中有0.5 NA个电子转移时,析出0.5mol Cu2O
C. 正极的电极反应为Ag2O+2e- + H2O==2Ag+2OH-
D. 电池工作时,OH-离子浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物 H 是一种抗病毒药物,在实验室中利用芳香烃 A 制备 H 的流程如下图所示(部分反应条件已略去):
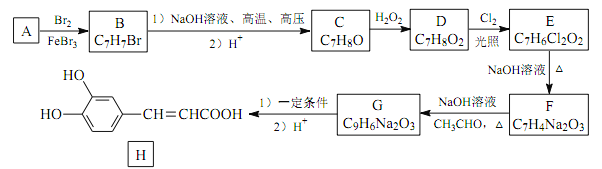
己知: ①有机物 B 苯环上只有两种不同环境的氢原子;
②两个羟基连在同一碳上不稳定,易脱水形成羰基或醛基;
③ RCHO + CH3CHO NaOH![]() RCH CHCHO + H2O;
RCH CHCHO + H2O;
④
(1)有机物 B 的名称为_____。
(2)由 D 生成 E 的反应类型为___________ , E 中官能团的名称为_____。
(3)由 G 生成 H 所需的“一定条件” 为_____。
(4)写出 B 与 NaOH 溶液在高温、 高压下反应的化学方程式:_____。
(5)F 酸化后可得 R, X 是 R 的同分异构体, X 能发生银镜反应,且其核磁共振氢谱显示有 3 种不同化学环境的氢,峰面积比为 1∶1∶1,写出 2 种符合条件的 X 的结构简式:_____。
(6)设计由 ![]() 和丙醛合成
和丙醛合成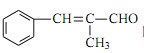 的流程图:_______________(其他试剂任选)。
的流程图:_______________(其他试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com