化学实验是研究物质性质的基础.
(1)下列有关实验操作或测量数据合理的是
(填序号).
a.用铁坩埚加热CuSO
4?5H
2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20mL的量筒,量取16.8mL的Na
2CO
3溶液
(2)某废水样品中含有一定的Na
+、CO
32-、SO
32-,甲、乙两研究小组欲测定其中SO
32-离子的浓度.
甲组方案:废水100mL
SO
固体
计算
试剂X从下列试剂中选择:
a.0.1mol?L
-1KMnO
4(H
2SO
4酸化)溶液b.0.5mol?L
-1NaOH溶液c.新制氯水d.KI溶液
①加入的试剂X为
(填字母序号),生成SO
42-主要的离子方程式为
.
②甲组方案中,第iii步的“系列操作”包含的操作名称各为
.
乙组方案:
i.用烧杯盛取废水适量,加少量活性炭,除去废水的杂色;过滤,取滤液;
ii.精确量取20.00mL过滤后废水试样,选择使用紫色的0.1mol?L
-1KMnO
4(H
2SO
4酸化)溶液进行滴定:(有关反应为:2MnO
4-+5SO
32-+6H
+=2Mn
2++5SO
42-+3H
2O
iii.记录数据,计算.
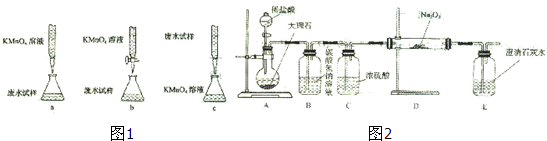
③乙组设计的下列滴定方式中,最合理的是(图1)
(夹持部分略去)(填字母序号)
(3)某同学制备Fe(OH)
3胶体:用洁净烧杯量 取适量蒸馏水加热至沸腾,向烧杯中缓慢滴加饱和的FeCl
3溶液,并不断用玻璃棒搅拦,结果溶液变浑浊.该同学制备胶体失败的原因是
,你认为成功制得Fe(OH)
3胶体的特征现象是
.
(4)用图2装置进行CO
2性质的有关实验.
①试剂瓶B中盛有饱和NaHCO
3溶液,其目的是
.
②反应过程中,E中澄清石灰水变浑浊,E中的混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系
.



