
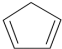
 )是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线:
)是一种重要的化工原料,下面是以环戊烷为原料制备环戊二烯的合成路线: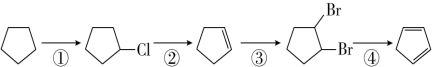
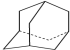 ),途径如下:
),途径如下: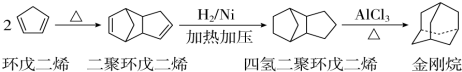
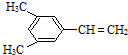 和
和 .
. 分析 (1)由合成路线可知,反应①为光照条件下的取代反应,反应②为在氢氧化钠醇溶液中加热发生消去反应,反应③为加成反应,反应④为在氢氧化钠醇溶液中加热发生消去反应,以此来解答;
(2)与双键碳直接相连的原子可以在同一平面内;
(3)结合有机物结构简式判断所含有的元素种类和原子个数可书写分子式;金刚烷中氢有两种:-CH-、-CH2-,利用等效氢,先固定一个氯原子,再移动另一个氯原子,据此判断异构体数目;
(4)能使溴的四氯化碳溶液褪色,应含有碳碳双键,其苯环上的一氯代物只有二种,说明苯环上只有两种氢,由此分析解答.
解答 解:(1)由合成路线可知,反应①为光照条件下的取代反应,反应②为在氢氧化钠醇溶液中加热发生消去反应生成环戊烯,反应③为加成反应,反应④为在氢氧化钠醇溶液中加热发生消去反应,反应①的产物名称为氯代环戊烷,反应②的反应试剂和反应条件为氢氧化钠醇溶液、加热,反应③的反应类型是加成反应,
故答案为:取代反应;氯代环戊烷;消去反应;环戊烯;
(2)碳碳双键为平面结构,与双键碳直接相连的原子可以在同一平面内,则5个C和4个H在同一平面内,故答案为:9;
(3)根据金刚烷的键线式可知,金刚烷分子中含有10个C、16个H,分子式为C10H16;金刚烷中氢有两种:-CH-、-CH2-,故二氯取代,可以固定一氯,移动另一氯,①固定-CH-,故另一氯可位于六元环的邻、间、对三种,②固定-CH2-,另一可位于同环的1号、3号碳位和异环的-CH2-位,三种,共6种,
故答案为:C10H16;6;
(4)能使溴的四氯化碳溶液褪色,应含有碳碳双键,所以可能的碳架结构为: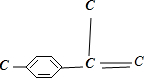 、
、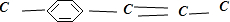 、
、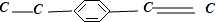 、
、 、
、 、
、 ,共6种,苯环上支链最多的几种同分异构体的结构简式:
,共6种,苯环上支链最多的几种同分异构体的结构简式: 和
和 ,故答案为:6;
,故答案为:6; 和
和 .
.
点评 本题考查有机物的合成及结构与性质,注意把握有机物的官能团、碳链骨架等的变化,明确发生的反应及习题中的信息即可解答,题目难度中等.


 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
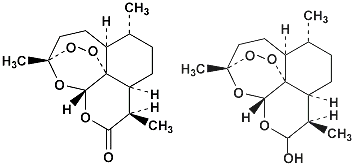
| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 由青蒿素制备双氢青蒿素的反应属还原反应 | |
| C. | 青蒿素分子中含有过氧链和酯基、醚键 | |
| D. | 双氢青蒿素分子中有2个六元环和2个七元环 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
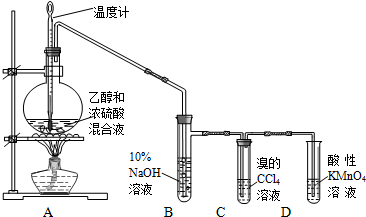 实验室制取乙烯并检验乙烯性质的装置如图.
实验室制取乙烯并检验乙烯性质的装置如图.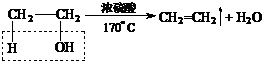 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9gD2O中含有的电子数为5NA | |
| B. | 1molMgCl2中含有的离子数为2NA | |
| C. | 1molCH4分子中共价键总数为4NA | |
| D. | 7.1gCl2与足量NaOH溶液反应转移的电子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色透明的溶液:Na+、Al3+、Cl-、OH- | |
| B. | pH=1的溶液:Na+、NH4+、Cu2+、NO3- | |
| C. | 与铝反应产生大量氢气的溶液:Na+、K+、Cl-、Al3+ | |
| D. | 使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu | B. | Fe | C. | Zn | D. | Al |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | 只有①②③ | C. | 只有①②③④ | D. | 都可以 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com