
| A. | 一定含有SO42- | B. | 一定含有Ag+ | ||
| C. | 一定含有Ag+和SO42- | D. | 可能含有Ag+或SO42- |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| 操作和现象 | 结论 | |
| A | 向NaCl溶液中先滴加少量AgNO3溶液,后滴加少量NaI溶液,先有白色沉淀,后变成黄色沉淀 | 说明Ksp(AgI)<Ksp(AgCl) |
| B | 将SO2通入酸性KMnO4溶液中,紫色褪去 | 说明SO2具有漂白性 |
| C | 向FeCl3和CuCl2混合溶液中加入铁粉,有红色固体析出 | 说明氧化性:Cu2+>Fe3+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有Ag+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从结构上推断,木糖分子中有多个羟基,因而能溶于水 | |
| B. | 木糖属于单糖 | |
| C. | 木糖属还原性糖,1mol木糖与足量的银氨溶液完全反应可生成108g银 | |
| D. | 木糖能发生酯化、氧化、加成等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
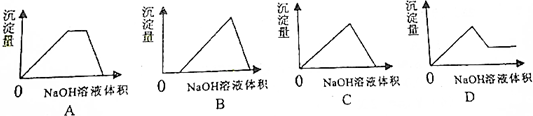
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 微粒符号 | 化学键类型 | 化合物类型 |
| HCl | 共价键 | 共价键化合物 |
| NaCl | 离子键 | 离子化合物 |
| NaOH | 离子键和共价键 | 离子化合物 |
| NH4Cl | 离子键和共价键 | 离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表有7个主族和8个副族 | B. | ⅣA族的元素全部是非金属元素 | ||
| C. | 元素周期表有7个周期 | D. | 短周期指第1、2周期 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com