
下列反应所得的溶液中一定只含一种溶质的是( )
|
| A. | 向硫酸酸化的Fe2(SO4)3溶液中加入过量的Ba(OH)2溶液 |
|
| B. | 向AlCl3溶液中加入过量的氨水 |
|
| C. | 向NaOH溶液中通人CO2气体 |
|
| D. | 将过量的Cu粉加入FeCl3溶液 |
| 铁盐和亚铁盐的相互转变;镁、铝的重要化合物. | |
| 专题: | 元素及其化合物. |
| 分析: | A.向硫酸酸化的Fe2(SO4)3溶液中,加入Ba(OH)2溶液时,OH﹣先和硫酸电离出的H+反应,然后再与Fe3+反应; B.氢氧化铝只能溶解在强酸和强碱中,不溶于弱碱氨水中; C.NaOH和CO2气体反应,先生成碳酸钠,再生成碳酸氢钠; D.氯化铁溶液跟铜反应,+3价的铁离子具有氧化性,单质铜具有还原性; |
| 解答: | 解: A.向硫酸酸化的Fe2(SO4)3溶液中,加入Ba(OH)2溶液时,硫酸先和氢氧化钡反应:H2SO4+Ba(OH)2=BaSO4↓+2H2O,再与Fe2(SO4)3反应,反应为:Fe2(SO4)3+3Ba(OH)2﹣=3BaSO4↓+2Fe(OH)3↓,反应所得的溶液中只含一种溶质是过量的Ba(OH)2.故A正确; B.氨水是弱碱,不能溶解氢氧化铝,氯化铝溶液加入过量氨水的反应方程式为:AlCl3+3NH3•H2O═Al(OH)3↓+3NH4Cl,反应所得的溶液中溶质为过量的氨水和产物NH4Cl,故B错误; C.NaOH和CO2气体反应,反应为:CO2+2NaOH=Na2CO3+H2O,再通入CO2气体CO2+Na2CO3+H2O=2NaHCO3,溶液中的溶质可能为Na2CO3、NaHCO3或Na2CO3或Na2CO3.故C错误; D.氯化铁溶液跟铜反应,+3价的铁离子被还原成+2价的铁离子,铜单质被氧化成+2价的铜离子,2FeCl3+Cu=CuCl2+2FeCl2,溶液中的溶质为CuCl2和FeCl2.故D错误; 故选A. |
| 点评: | 该题反应所得的溶液中一定只含一种溶质与加入反应物的量有关,较复杂.做这类题目要分情况讨论,根据反应,写出正确的方程式求解. |


科目:高中化学 来源: 题型:
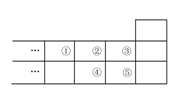
右图是元素周期表的一部分,下列说法中正确的是( )
A.元素①位于第二周期第ⅣA族
B.气态氢化物的稳定性:④>②
C.最高价氧化物对应水化物酸性:⑤>④
D.元素的最高正化合价:③=⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A.非金属气态氧化物都不是电解质 B.SO2、NO2、C02都会导致酸雨的形成
C.氮的氧化物都属于大气污染物 D.Si、S的氧化物均属于酸性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡,混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下方案:
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(1)该反应的离子方程式为 ;
(2)探究温度对化学反应速率影响的实验编号是 (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是 ;
(3)实验①测得KMn04溶液的褪色时间为40 s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMn04)= mol·L-1·min-1;
(4)已知50℃时c(MnO4-)~反应时间t的变化曲线如图。若保持其他条件不变,请在坐标图中,画出25℃时c(Mn04-)~t的变化曲线示意图。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的化学方程式或离子方程式不正确的是( )
|
| A. | 向饱和Na2CO3中加入过量CO2气体:CO32﹣+CO2+H2O=2HCO3﹣ |
|
| B. | 在沸水中滴入饱和FeCl3溶液制取Fe(OH)3胶体:Fe3++3H2O=Fe(OH)3(胶体)+3H+ |
|
| C. | 4mol/L的NaAlO2溶液和7mol/L的盐酸等体积混合:4AlO2﹣+7H++H2O=3Al(OH)3↓+Al3+ |
|
| D. | 酸化的KMnO4溶液与H2O2反应:2MnO4﹣+6H++5H2O2=2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
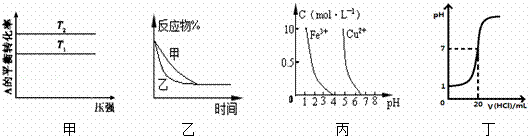
下列图示与对应的叙述相符的是( )
|
| A. | 图甲可以判断出反应A(g)+B(g)⇌若2C(g)的△H<0,T2>T1 |
|
| B. | 图乙表示压强对可逆反应2A(g)+2B(g)⇌3C(g)+D(s)的影响.乙的压强比甲的压强大 |
|
| C. | 依据图丙,若除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调节pH≈4 |
|
| D. | 图丁表示25℃时,用0.1 mol/L叫盐酸滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入盐酸体积的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g)⇌xC(g)+D(s),向甲中通入6mol A和2mol B,向乙中通入1.5mol A、0.5mol B和3mol C和2mol D,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是( )
|
| A. | 若平衡时,甲、乙两容器中A的物质的量不相等,则x=4 |
|
| B. | 平衡时,甲、乙两容器中A、B的物质的量之比不相等 |
|
| C. | 平衡时甲中A的体积分数为40% |
|
| D. | 若平衡时两容器中的压强不相等,则两容器中压强之比为8:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列实验的描述正确的是( )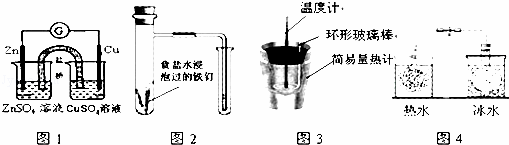
|
| A. | 图1所示的实验:根据电流计(G)中指针是否偏转即可比较Zn、Cu的金属活泼性 |
|
| B. | 图2所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀 |
|
| C. | 图3所示的实验:根据温度计读数的变化测定稀硫酸和NaOH溶液反应的反应热 |
|
| D. | 图4所示的实验:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)判断2NO2(g)⇌N2O4(g)是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.苯和溴水振荡后,由于发生化学反应而使溴水的水层颜色变浅
B.酸性高锰酸钾溶液和溴水都既能鉴别出甲烷和乙烯又能除去甲烷中含有的乙烯再经干燥而获得纯净的甲烷
C.煤中含有苯和甲苯,可以用先干馏,后蒸馏的方法把它们分离出来
D.石油中含有C5~C11的烷烃,可以通过分馏得到汽油
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com