
| A. | ①③④ | B. | ①②③ | C. | ①②④ | D. | ②④ |
分析 新制氯水中含有含有三种分子:Cl2、H2O、HClO,四种离子:H+、Cl-、ClO-及少量OH-;久置后发生反应Cl2+H2O?HCl+HClO,2HClO═2HCl+O2↑,由于HClO的分解导致了Cl2的不断反应,最后变成了HCl溶液,这时溶液中含有H2O、H+、Cl-及少量的H+,减少的为Cl2、H2O、HClO.
解答 解:氯气的水溶液称为氯水,新制氯水呈黄绿色,有刺激性气味,在氯水中存在如下三个平衡:Cl2+H2O?HCl+HClO,HClO?H++ClO-,H2O?H++OH-,
所以新制的氯水中含有三种分子:Cl2、H2O、HClO,四种离子:H+、Cl-、ClO-及少量OH-;
久置后发生反应:Cl2+H2O?HCl+HClO,2HClO═2HCl+O2↑,由于HClO的分解导致了Cl2的不断反应,最后变成了HCl溶液,所以减少的是①Cl2、②H2O、④HClO.
故选C.
点评 本题考查新制氯水和久置氯水的成分的不同,新制氯水含有氯气和次氯酸,具有酸性、漂白性和强氧化性,题目难度中等.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:实验题
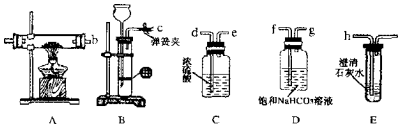
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
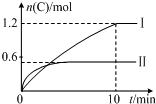 在2L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g)?2C(g)+D(s)△H=akJ•mol-1实验内容和结果分别如表和如图所示.下列说法正确的是( )
在2L的恒容密闭容器中充入A(g)和B(g),发生反应:A(g)+B(g)?2C(g)+D(s)△H=akJ•mol-1实验内容和结果分别如表和如图所示.下列说法正确的是( )| 实验 序号 | 温度 | 起始物质的量 | 热量 变化 | |
| A | B | |||
| Ⅰ | 600℃ | 1mol | 3mol | 96kJ |
| Ⅱ | 800℃ | 1.5mol | 0.5mol | ─ |
| A. | a=-160 | |
| B. | 600℃时,该反应的平衡常数是0.45 | |
| C. | 实验Ⅰ中,10min内平均速率v(B)=0.06mol•L-1•min-1 | |
| D. | 向实验Ⅱ的平衡体系中再充入0.5molA和1.5molB,A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol Na2CO3和1mol NaOH | B. | 1mol Na2CO3和2mol NaOH | ||
| C. | 2mol Na2CO3和2mol NaOH | D. | 2mol Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 199F- | B. | 1910Ne | C. | 2910F | D. | 2919K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “物质的量”是国际单位制对一个基本单位 | |
| B. | 1mol任何物质均含有6.02×1023个分子 | |
| C. | 物质对摩尔质量等于其其相对分子质量或相对原子质量 | |
| D. | 0.012kg12C中所含对碳原子数为NA(NA代表阿伏加德罗常数对数值) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2和O2反应生成水 | B. | 锌片投入稀硫酸中生成H2 | ||
| C. | H2O2分解制取O2 | D. | NH3遇到HCl气体生成白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 配制2.0 mol•L-1的Na2CO3溶液950 mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为950 mL和201.4 g | |
| B. | 标准状况下,用3.36L HCl气体做喷泉实验完毕后,液体冲入烧瓶的一半(假设实验过程溶液无泄漏),溶液中溶质的物质的量浓度为$\frac{1}{22.4}$mol/L | |
| C. | 向0.1mol•L-1 CH3COOH溶液中加入少量水,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 | |
| D. | 将溶质相同质量分数分别为3p%的溶液和p%的溶液等体积混合得到质量分数为q%的溶液,则p、q的关系不可能为q>2p |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com